Типы химических связей
В химии атомы редко существуют поодиночке. Они объединяются в молекулы и кристаллы с помощью химических связей.
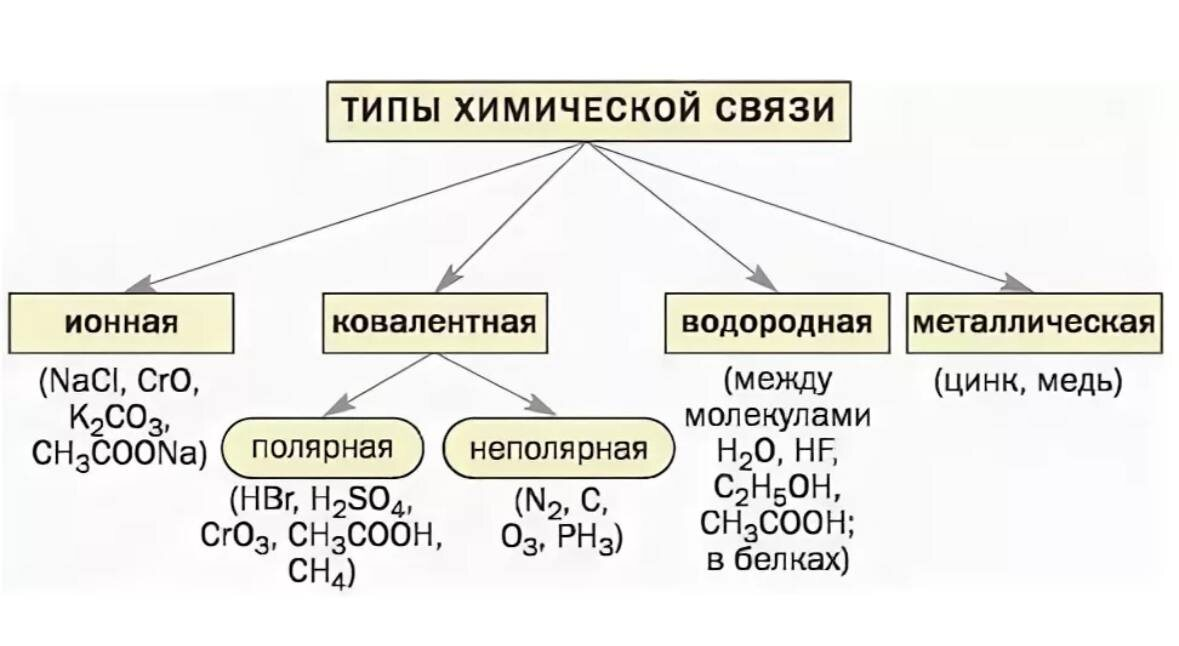
1. Ковалентная химическая связь
Определение
Ковалентная химическая связь — это химическая связь, образующаяся за счёт обобществления электронных пар (перекрывания атомных орбиталей). Возникает, как правило, между атомами неметаллов.
Классификация
Неполярная связь
Образуется между атомами одного элемента с одинаковой электроотрицательностью (ΔЭО = 0).
- Простые вещества: H2, O2, N2, F2, Cl2, Br2, I2, P4, S8.
- Сложные вещества (связь между
одинаковыми атомами):
- Пероксид водорода H2O2 (связь O–O)
- Пирит FeS2 (связь S–S)
- Карбид кальция CaC2 (связь C≡C)
- Органика (этан C2H6, бензол C6H6 — связи C–C)
Полярная связь
Образуется между атомами разных неметаллов (ΔЭО > 0, но < 1.7). Электронная плотность смещена к более электроотрицательному атому.
- Примеры: HCl, H2O, NH3, CO2, SO3, P2O5, CCl4, OF2.
Запомните: Чем больше разница электроотрицательностей атомов, тем более полярной является связь!
Механизмы образования
Существует два основных механизма образования ковалентной связи:
Обменный механизм
Каждый атом предоставляет по одному неспаренному электрону на образование общей связи.
A• + •B → A:B
Донорно-акцепторный механизм
Один атом (донор) предоставляет неподеленную электронную пару, а другой (акцептор) — свободную орбиталь.
A: + □B → A:B (или A→B)
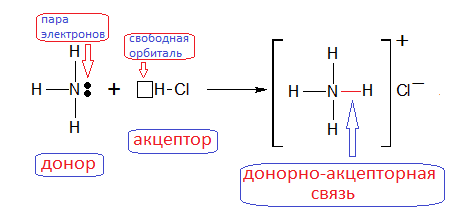
- Ион аммония NH4+ (и его соли)
- Угарный газ CO
- Азотная кислота HNO3 и нитраты
- Комплексные соединения (напр., Na[Al(OH)4])
- Озон O3
- Оксид азота (V) N2O5
Характеристики ковалентной связи
Основные параметры связи — это длина, энергия и кратность. Они тесно взаимосвязаны.
1. Зависимость от кратности связи
Чем выше кратность связи, тем она короче и тем она прочнее (энергия разрыва выше).
| Тип связи | Пример | Длина, пм | Энергия, кДж/моль |
|---|---|---|---|
| Одинарная (σ) | C—C | 154 | 343 |
| Двойная (σ+π) | C=C | 134 | 615 |
| Тройная (σ+2π) | C≡C | 120 | 812 |
Вывод: Чем выше кратность, тем короче и прочнее связь
2. Кратность связи в простых веществах
| Кратность | Связь | Примеры |
|---|---|---|
| 1 | H–H, Cl–Cl | H2, F2, Cl2, Br2, I2 |
| 2 | O=O | O2 |
| 3 | N≡N | N2 |
3. Зависимость от радиуса атома
| Связь | Длина | Прочность | Кислотность |
|---|---|---|---|
| H—F | 0.092 нм (самая короткая) | 565 кДж/моль (самая прочная) | Слабая кислота |
| H—Cl | 0.127 нм | 431 кДж/моль | Сильная кислота |
| H—Br | 0.141 нм | 364 кДж/моль | Сильная кислота |
| H—I | 0.161 нм (самая длинная) | 297 кДж/моль (наименее прочная) | Сильнейшая кислота |
Вывод: С ростом радиуса атома связь удлиняется, ослабевает, а кислотность растет
2. Ионная химическая связь
Определение
Ионная связь — это сильное электростатическое притяжение между разноименно заряженными ионами. Возникает между элементами с большой разницей электроотрицательностей (обычно это Металл + Неметалл), а также в солях аммония.
Где встречается ионная связь?
Бинарные соединения
(Металл + Галоген/Кислород/Сера)
- NaCl, K2O, CaF2, LiBr, MgO
Соли с кислородом
(Между металлом и кислотным остатком)
- Na2SO4, CaCO3, KNO3
Щелочи
(Между металлом и OH-группой)
- NaOH, Ba(OH)2, KOH
Соли аммония
(Без металлов! Ионная связь между катионом NH₄⁺ и анионом)
- NH4Cl, (NH4)2SO4
3. Металлическая связь
Определение
Металлическая связь — это особая связь в металлах и сплавах, которая образуется за счёт обобществления валентных электронов. В узлах кристаллической решетки металлов находятся катионы и нейтральные атомы, а между ними свободно перемещаются «электронный газ».
- Электропроводность
- Теплопроводность
- Пластичность и ковкость
- Характерный металлический блеск
Примеры веществ:
- Все чистые металлы:
Fe (железо), Cu (медь), Na (натрий), Au (золото), Al (алюминий), Zn, Mg, Ti и т.д. - Все сплавы:
Бронза, Латунь, Сталь, Чугун, Дюралюминий, Мельхиор.
4. Водородная связь
Определение
Водородная связь — это межмолекулярное (редко внутримолекулярное) взаимодействие между электроположительным атомом Водорода (H) одной молекулы и сильно электроотрицательным атомом (F, O, N) другой молекулы.
Как быстро узнать молекулу с H-связью:
Если в молекуле есть связи H-F, H-O, H-N — значит, вещество образует водородные связи!
Примеры:
- H2O (Вода)
- HF (Фтороводород)
- NH3 (Аммиак)
- R-OH (Спирты)
- R-COOH (Карбоновые к-ты)
- Белки и ДНК
Водородные связи объединяют молекулы, повышая температуру кипения и растворимость в воде.
5. Уловки и ловушки ЕГЭ
Скрытая ковалентная неполярная связь
Ее часто забывают найти в сложных и органических веществах:
- Пероксиды (Na2O2, H2O2): есть связь O–O.
- Ацетилениды (CaC2), карбиды: связь C≡C.
- Пирит (FeS2): связь S–S.
- Любая органика с 2+ атомами C: связь C–C (кроме метана).
Скрытая ионная связь
Во многих солях, которые кажутся «чисто органическими», есть ионная связь!
- Соли карбоновых кислот: ацетат натрия (CH3COONa) — ИОННАЯ связь между Na⁺ и анионом.
- Соли аминов: хлорид метиламмония [CH3NH3]Cl.
- Алкоголяты и феноляты: CH3ONa.
«Все виды связей сразу»
Типичное задание: «Выберите вещества, в которых есть и ионная, и ковалентная полярная связь».
Что искать?
- Соли кислородсодержащих кислот (K2SO4, NaNO3)
- Щёлочи (NaOH, KOH)
- Соли аммония (NH4Cl, (NH4)2SO4)
Пройди тест по теме
Проверь свои знания по типам химической связи. Задания формата ЕГЭ.