Кристаллические решетки и строение вещества
1. Аморфные и кристаллические вещества
Твердые вещества делятся на две большие группы в зависимости от упорядоченности внутреннего строения:
Определение
Кристаллические вещества — частицы строго упорядочены и образуют правильную пространственную кристаллическую решетку (каркас).
- Имеют строгую постоянную температуру плавления.
- При ударе раскалываются по определенным плоскостям (образуя ровные плоские грани).
Примеры: Алмаз, лёд, поваренная соль, все чистые металлы (железо, золото).
Определение
Аморфные вещества — частицы расположены хаотично, без геометрического порядка. По внутреннему строению они похожи на очень густые, застывшие жидкости.
- Нет точной температуры плавления (при нагревании они постепенно размягчаются).
- При ударе образуют неровные осколки (раковистый излом).
Примеры: Стекло, смола, янтарь, пластилин, пластмассы и резина.
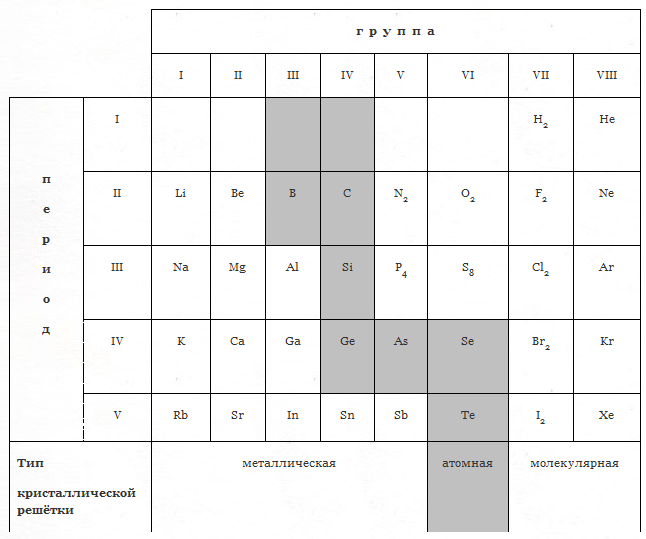
2. Типы кристаллических решёток
Физические свойства веществ (температура плавления, твердость, электропроводность) зависят от типа их кристаллической решетки.
| Тип решётки | Молекулярная | Атомная | Ионная | Металлическая |
|---|---|---|---|---|
| Тип связи | Ковалентная (внутри молекул) + Слабые межмолекулярные силы | Ковалентная (очень прочная) | Ионная | Металлическая |
| В узлах решетки | Молекулы | Атомы | Ионы (+ и -) | Атомы и ионы (в "электронном газе") |
| Свойства |
• Летучие (имеют запах) • Легкоплавкие (низкая Тпл) • Малая твердость • Диэлектрики (не проводят ток) |
• Очень твердые • Тугоплавкие (очень высокая Тпл) • Нелетучие • Нерастворимые |
• Твердые, но хрупкие • Тугоплавкие • Растворы и расплавы проводят ток • Часто растворимы в воде |
• Пластичные, ковкие • Металлический блеск • Высокая тепло- и электропроводность |
| Типичные примеры |
• Все газы (O2, N2, CO2) • Жидкости (H2O, Br2) • Твердые: I2, S8, P4 (белый), C60 (фуллерен) • Органика (почти вся) |
• C (алмаз, графит) • Si (кремний) • B (бор) • SiO2 (кремнезем, кварц, песок) • SiC (карборунд) |
• Соли (NaCl, K2SO4, NH4Cl) • Щелочи (NaOH, KOH) • Оксиды металлов (CaO, CuO) • Бинарные соединения Ме+НеМе |
• Металлы (Fe, Cu, Na, Au) • Сплавы (бронза, сталь) |
3. Молекулярное и немолекулярное строение
В зависимости от типа химической связи и кристаллической решетки, все вещества можно разделить на две группы по строению.
1. Вещества молекулярного строения
Состоят из молекул. Внутри молекул связи очень прочные (ковалентные), но между самими молекулами действуют слабые межмолекулярные силы.
Основные свойства
- Легкоплавкие: низкие температуры плавления и кипения.
- Летучие: часто имеют характерный запах.
- Диэлектрики: слабая электропроводность.
- Агрегатное состояние (студ. усл.): к ним относятся все газы и жидкости (кроме ртути), а также некоторые твердые вещества.
Примеры веществ
- Газы: H2, O2, Cl2, N2, CO2, NH3
- Жидкости: H2O, H2SO4 (безводная), Бром (Br2)
- Твердые вещества: Йод (I2), Сера (S8), Белый фосфор (P4), Глюкоза, Сахароза
2. Вещества немолекулярного строения
Не содержат молекул. Атомы или ионы связаны в единый бесконечный каркас (кристаллическую решетку).
Основные свойства
- Тугоплавкие: высокие температуры плавления.
- Твердые: высокая твердость и механическая прочность.
- Нелетучие: не имеют запаха.
Типы связей и решеток
- Ионная решетка: Соли (NaCl), Щелочи (NaOH), Оксиды металлов (CaO).
- Металлическая решетка: Все металлы и сплавы.
- Атомная решетка (ковалентная): Алмаз (C), Графит (C), Кремний (Si), Кварц (SiO2), Карбид кремния (SiC).
Особые случаи и исключения для ЕГЭ
Оксиды металлов
Обычно оксиды металлов имеют ионную решетку (CaO, CuO), но оксиды металлов в высоких степенях окисления (+5, +6, +7) являются кислотными оксидами и имеют молекулярную решетку!
Примеры: CrO3 (оксид хрома VI), Mn2O7 (оксид марганца VII).
Органические соли
Органические вещества обычно имеют молекулярную решетку. Но соли органических кислот, аминокислот и аминов имеют ионную решетку.
Примеры: CH3COONa (ацетат натрия), C6H5ONa (фенолят натрия), [CH3NH3]Cl (хлорид метиламмония).
Аллотропные модификации
Один и тот же химический элемент может образовывать совершенно разные кристаллические решетки:
- Углерод: Алмаз, графит — атомная. Фуллерен — молекулярная (C60).
- Фосфор: Красный, черный — атомная. Белый — молекулярная (P4).
Пройди тест по теме
Проверь свои знания по кристаллическим решеткам. Задания формата ЕГЭ.