Электролиз расплавов и растворов
Темы кодификатора ЕГЭ: Электролиз солей, щелочей, кислот. Катодные и анодные процессы. Получение веществ электролизом.
1. Что такое электролиз?
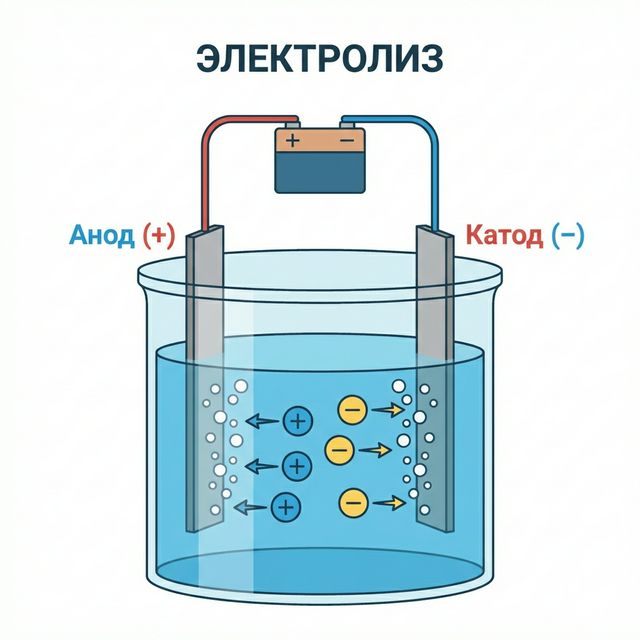
В процессе участвуют два электрода:
Заряд электрода: Отрицательный (−)
Кто движется: Катионы (+)
Процесс: Восстановление (приём e⁻)
Пример:
Cu²⁺ + 2e⁻ → Cu⁰
Заряд электрода: Положительный (+)
Кто движется: Анионы (−)
Процесс: Окисление (отдача e⁻)
Пример:
2Cl⁻ − 2e⁻ → Cl₂⁰
2. Электролиз расплавов
В расплавах нет воды, поэтому окисляются и восстанавливаются только ионы самого вещества.
Правило: Катион металла восстанавливается до чистого металла, анион кислотного остатка окисляется до простого вещества.
Диссоциация: NaCl → Na⁺ + Cl⁻
Катод (−): Na⁺ + 1e⁻ → Na⁰ (восстановление)
Анод (+): 2Cl⁻ − 2e⁻ → Cl₂⁰ (окисление)
Суммарно: 2NaCl (расплав) ⎯⎯эл.ток⎯→ 2Na + Cl₂↑
Электролизом расплавов получают активные металлы (Li, Na, K, Ca, Al и др.) и фтор.
Алюминий получают электролизом расплава оксида алюминия (Al₂O₃) в криолите (Na₃[AlF₆]).
2Al₂O₃ ⎯⎯⎯криолит⎯→ 4Al + 3O₂↑
3. Электролиз растворов: катодные и анодные процессы
В видных растворах, помимо ионов электролита (соли, щелочи, кислоты), присутствуют молекулы воды (H₂O). Вода является слабым электролитом, но она также способна окисляться и восстанавливаться.
Именно конкуренция между ионами и водой определяет продукты реакции.
3.1. Процессы на КАТОДЕ (−)
Катод — это «восстановитель». Он отдает электроны катионам.
Процесс на катоде не зависит от материала катода. Он зависит от положения металла катиона в электрохимическом ряду напряжений.
Восстанавливается ТОЛЬКО вода Средние
Восст. МЕТАЛЛ + ВОДА Неактивные
Восстанавливается ТОЛЬКО металл
| Активные металлы (Li ... Al) |
Металлы средней
активности (Mn ... Pb) |
Неактивные
металлы (Cu ... Au) |
|---|---|---|
|
Li⁺, K⁺, Rb⁺, Cs⁺, Ca²⁺, Sr²⁺, Ba²⁺, Na⁺,
Mg²⁺, Al³⁺ (а также NH₄⁺) Катион металла НЕ восстанавливается. Восстанавливается вода:
2H₂O + 2e⁻ → H₂↑ + 2OH⁻
|
Mn²⁺, Zn²⁺, Cr³⁺, Fe²⁺, Cd²⁺, Co²⁺, Ni²⁺,
Sn²⁺, Pb²⁺
Идут два процесса одновременно: 1. Восстановление металла: Meⁿ⁺ + ne⁻ → Me⁰ 2. Восстановление воды: 2H₂O + 2e⁻ → H₂↑ + 2OH⁻ |
Cu²⁺, Hg²⁺, Ag⁺, Pt²⁺, Au³⁺
Восстанавливается только металл. Вода химически не взаимодействует.
Meⁿ⁺ + ne⁻ → Me⁰
|
При электролизе растворов кислот на катоде всегда восстанавливаются ионы водорода:
2H⁺ + 2e⁻ → H₂↑
3.2. Процессы на АНОДЕ (+)
Анод — это «окислитель» (забирает электроны). Процесс зависит от того, из чего сделан сам анод, и от природы анионов.
А) Если анод РАСТВОРИМЫЙ (Cu, Zn, Fe, Ag и др.)
Анионы раствора не окисляются.
Окисляется материал самого анода (металл посылает электроны во внешнюю цепь и переходит в раствор в виде ионов).
Уравнение: Me⁰ − ne⁻ → Meⁿ⁺
Пример: Электролиз CuSO₄ с медным анодом (рафинирование меди).
Б) Если анод ИНЕРТНЫЙ (Графит C, Платина Pt, Золото Au)
Материал анода не реагирует. Идет конкуренция между анионами и водой.
| 1
группа Бескислородные |
2
группа Кислородсодержащие + F⁻ |
3
группа Гидроксиды (OH⁻) |
|---|---|---|
|
1. Анионы бескислородных кислот (кроме F⁻) S²⁻, I⁻, Br⁻, Cl⁻ Окисляется сам анион. S²⁻ − 2e⁻ → S⁰↓ (осадок серы) 2I⁻ − 2e⁻ → I₂↓ (бурый осадок/р-р) 2Br⁻ − 2e⁻ → Br₂ (бурая жидкость) 2Cl⁻ − 2e⁻ → Cl₂↑ (желто-зеленый газ) |
2. Анионы кислородсодержащих кислот и F⁻ SO₄²⁻, NO₃⁻, PO₄³⁻, CO₃²⁻, SiO₃²⁻, ClO₄⁻, F⁻ Окисляется ВОДА. Анион не изменяется. 2H₂O − 4e⁻ → O₂↑ + 4H⁺ (Выделяется кислород, среда становится кислой) |
3. Гидроксид-ионы OH⁻ (в растворах щелочей) NaOH, KOH, Ba(OH)₂ Окисляется OH-группа. 4OH⁻ − 4e⁻ → O₂↑ + 2H₂O (Выделяется кислород) |
|
4. Анионы органических кислот (R-COO⁻) CH₃COO⁻, C₂H₅COO⁻ и др. Реакция Кольбе: Окисление с декарбоксилированием (отщепление CO₂). Образуется углекислый газ, а радикалы соединяются (удваиваются).
Общая схема:
2R–COO⁻ − 2e⁻ → R–R + 2CO₂↑
Пример (Ацетат натрия):
2CH₃COO⁻ − 2e⁻ → C₂H₆↑ (этан) + 2CO₂↑
Пример (Пропионат калия):
2C₂H₅COO⁻ − 2e⁻ → C₄H₁₀ (бутан) + 2CO₂↑ |
||
4. Электролитические способы получения веществ
Электролиз — один из промышленных способов получения чистых веществ. Важно помнить, что можно получить из раствора, а что — только из расплава.
| Получаемое вещество | Способ получения | Пример уравнения |
|---|---|---|
| Щелочные и щел.-зем. металлы (Li, Na, K, Ca, Ba...) |
Электролиз РАСПЛАВОВ солей (обычно хлоридов). Из раствора их получить НЕЛЬЗЯ (выделяется H₂). |
2NaCl(расплав) → 2Na + Cl₂↑ |
| Алюминий (Al) | Электролиз РАСПЛАВА оксида Al₂O₃ в криолите. Хлорид алюминия возгоняется, его не используют. |
2Al₂O₃ (криолит) → 4Al + 3O₂↑ |
| Металлы средней активности и неактивные (Zn, Cr, Fe, Ni, Cu, Ag...) |
Электролиз РАСТВОРОВ солей. | 2CuSO₄ + 2H₂O → 2Cu + O₂ + 2H₂SO₄ |
| Щелочи (NaOH, KOH) | Электролиз РАСТВОРОВ хлоридов активных металлов (Na, K). | 2NaCl + 2H₂O → H₂↑ + Cl₂↑ + 2NaOH |
| Галогены (Cl₂, Br₂, I₂) | Электролиз РАСТВОРОВ (или расплавов) галогенидов. | 2NaCl + 2H₂O → H₂ + Cl₂ + 2NaOH |
| Фтор (F₂) | Электролиз РАСПЛАВОВ фторидов. Из раствора получить нельзя (окисляется вода). |
2KF(расплав) → 2K + F₂↑ |
| Водород (H₂) и Кислород (O₂) | Электролиз РАСТВОРОВ кислородсодержащих солей активных металлов или щелочей (фактически — электролиз воды). | 2H₂O → 2H₂↑ + O₂↑ |
5. Примеры реакций электролиза растворов
1. Хлорид натрия (NaCl)
Соль образована активным металлом (Na) и бескислородным остатком (Cl).
- Катод: (Na ← активный) → восстанавливается вода (2H₂O + 2e⁻ → H₂ + 2OH⁻)
- Анод: (Cl без O) → окисляется хлор (2Cl⁻ − 2e⁻ → Cl₂)
В растворе остаются ионы Na⁺ и OH⁻ → образуется щелочь NaOH.
2NaCl + 2H₂O ⎯⎯эл.ток⎯→ H₂↑ + Cl₂↑ + 2NaOH
2. Сульфат меди (II) (CuSO₄)
Соль образована малоактивным металлом (Cu) и кислородсодержащим остатком (SO₄).
- Катод: (Cu ← неактивный) → восстанавливается медь (Cu²⁺ + 2e⁻ → Cu)
- Анод: (SO₄ с кислородом) → окисляется вода (2H₂O − 4e⁻ → O₂ + 4H⁺)
В растворе остаются ионы H⁺ и SO₄²⁻ → образуется серная кислота H₂SO₄.
2CuSO₄ + 2H₂O ⎯⎯эл.ток⎯→ 2Cu↓ + O₂↑ + 2H₂SO₄
3. Нитрат калия (KNO₃)
Соль образована активным металлом (K) и кислородсодержащим остатком (NO₃).
- Катод: (K ← активный) → восстанавливается вода (выделяется H₂)
- Анод: (NO₃ с кислородом) → окисляется вода (выделяется O₂)
Соль не расходуется, происходит только электролиз воды!
2H₂O ⎯⎯эл.ток⎯→ 2H₂↑ + O₂↑