Реакции ионного обмена
1. Что такое реакции ионного обмена?
Определение
Реакции ионного обмена (РИО) — это реакции, которые протекают между ионами в растворе электролитов без изменения степеней окисления элементов.
РИО тесно связаны с понятием электролитической диссоциации — процессом распада вещества на ионы (заряженные частицы) в растворе или расплаве.
Важно
В реакциях ионного обмена степени окисления элементов НЕ меняются. Это главное отличие РИО от окислительно-восстановительных реакций (ОВР).
Механизм растворения
При растворении вещества с ионной связью (например, $NaCl$) в воде происходит следующее:
- Молекулы воды являются диполями (имеют положительный и отрицательный полюса).
- Диполи воды окружают ионы соли: положительные концы притягиваются к анионам ($Cl^-$), отрицательные — к катионам ($Na^+$).
- Связь между ионами в кристалле ослабевает, и они переходят в раствор в виде гидратированных ионов.
2. Условия протекания РИО
Не все вещества способны реагировать друг с другом. Для протекания реакции должны выполняться определенные условия как для реагентов, так и для продуктов.
Условия для реагентов
Реагенты в большинстве случаев должны быть растворимы (Р + Р).
Условия для продуктов
В продуктах должен образоваться:
- Осадок
- Газ
- Вода или слабая кислота
2.1. Условия для реагентов (подробно)
Основное правило
Оба реагента должны быть растворимы в воде (смотрим таблицу растворимости).
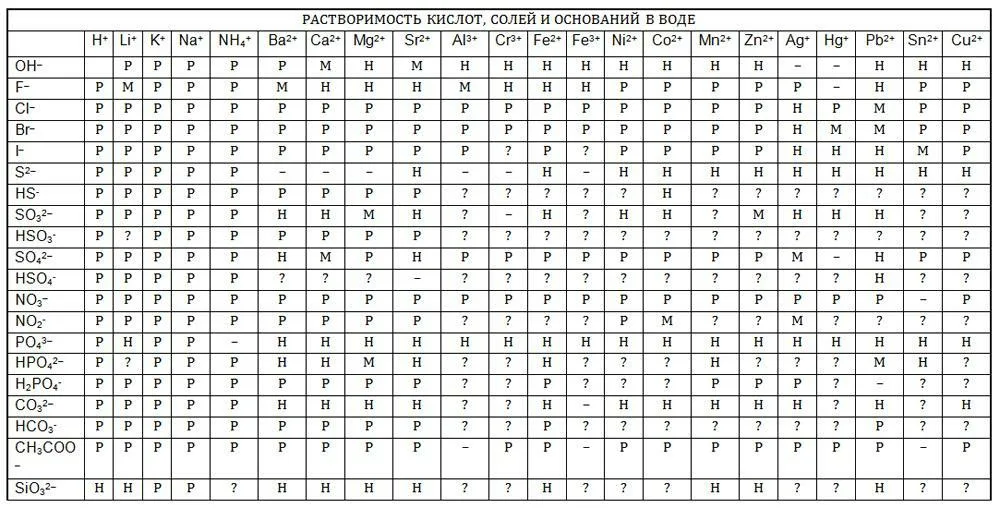
Исключения из правила растворимости
1. Кислоты + нерастворимые соли:
Кислоты способны реагировать с малорастворимыми и некоторыми нерастворимыми солями, кроме пятерки сульфидов: $Ag_2S$, $PbS$, $CuS$, $CdS$, $HgS$.
2. Гидроксиды могут быть нерастворимы:
Кислота должна быть растворимой, а гидроксид может быть любым:
$Al(OH)_3 + 3HCl \to AlCl_3 + 3H_2O$
3. Нерастворимые кислоты:
Нерастворимые кислоты реагируют только со щелочами:
«Матрёшка» исключений для сероводорода
Соли пятерки металлов (Cu, Ag, Hg, Cd, Pb) способны реагировать со слабой сероводородной кислотой $H_2S$, так как образующийся сульфид нерастворим и не реагирует с образовавшейся кислотой:
2.2. Условия для продуктов (подробно)
Реакция ионного обмена протекает, если в результате образуется:
1. Газ или неустойчивое вещество
$H_2CO_3 \to H_2O + CO_2\uparrow$ | $H_2SO_3 \to H_2O + SO_2\uparrow$ | $NH_3 \cdot H_2O \to NH_3\uparrow + H_2O$
2. Осадок или неустойчивое вещество
$2AgOH \to Ag_2O\downarrow + H_2O$ | $Hg(OH)_2 \to HgO\downarrow + H_2O$
$2AgF + 2KOH \to 2KF + Ag_2O\downarrow + H_2O$
3. Вода или слабый электролит
Образование воды — признак реакции нейтрализации:
$NaHCO_3 + NaOH \to Na_2CO_3 + H_2O$
3. Молекулярные и ионные уравнения
Реакции ионного обмена можно записать тремя способами:
Молекулярное уравнение
Уравнение с незаряженными атомами и молекулами.
Полное ионное уравнение
Уравнение с ионами, образовавшимися при диссоциации.
Сокращённое ионное уравнение
Получается путём сокращения одинаковых ионов слева и справа.
Что расписываем на ионы, а что нет?
В ионных уравнениях записывают в виде ионов формулы:
- растворимых солей;
- сильных кислот (HCl, HBr, HI, HNO3, HClO3, HClO4, H2SO4 и др.);
- сильных оснований (щелочи LiOH, NaOH, KOH, CsOH, RbOH, Ca(OH)2, Sr(OH)2, Ba(OH)2).
В ионных уравнениях записываются в виде молекул формулы:
в РИО не используем
- воды;
- слабых кислот (HF, H2S, H2SO3, H2CO3, H2SiO3, HNO2, HCN, H3PO4, HClO, HClO2, органические кислоты HCOOH, CH3COOH и др.);
- NH3 · H2O, нерастворимых оснований и амфотерных гидроксидов (Zn(OH)2, Fe(OH)2, Fe(OH)3, Al(OH)3, Cu(OH)2 и др.);
- газообразных веществ (CO2, H2S, NH3, SO2);
- нерастворимых солей.
Особенность малорастворимых гидроксидов
$Ca(OH)_2$ и $Sr(OH)_2$ — малорастворимы:
- В левой части уравнения — расписываем на ионы (если они исходные вещества в растворе)
- В правой части уравнения — НЕ расписываем (осадок)
$Ca^{2+} + 2OH^- \to Ca(OH)_2\downarrow$
Запомните
Указывайте заряд иона (сначала число, потом знак): $Ca^{2+}$. Не путайте со степенью окисления (сначала знак, потом число): $Ca^{+2}$
4. Алгоритм составления ионных уравнений (ЕГЭ)
В списке веществ находим два вещества, между которыми будет протекать реакция ионного
обмена.
Не забывайте про исключения!
Записываем уравнение реакции в молекулярном виде.
Не забывайте уравнивать коэффициенты!
Расписываем на ионы все вещества, которые диссоциируют.
Не забывайте писать заряды ионов!
Сокращаем одинаковые ионы в левой и правой частях.
Не забывайте сокращать коэффициенты!
Примеры решения задач ЕГЭ (Задание 30)
Задача 1. Реакция с выделением газа
РешениеУсловие: Из предложенного перечня веществ выберите вещества, между которыми протекает реакция ионного обмена с выделением газа. Запишите молекулярное, полное и сокращённое ионные уравнения реакции.
Перечень веществ: серная кислота, сульфит натрия, хлорид бария, нитрат калия, оксид меди(II).
Анализ веществ: $H_2SO_4$ — сильная кислота, $Na_2SO_3$ — растворимая соль, $BaCl_2$ — растворимая соль, $KNO_3$ — растворимая соль, $CuO$ — оксид, не электролит
Решение: Проверяем возможные пары:
- $H_2SO_4 + Na_2SO_3$ — образуется $H_2SO_3$, которая разлагается на $H_2O + SO_2\uparrow$ Газ!
- $H_2SO_4 + BaCl_2$ — образуется осадок $BaSO_4\downarrow$ (не газ)
- $H_2SO_4 + KNO_3$ — реакция не идёт (нет газа, осадка, воды)
Задача 2. Реакция с выпадением осадка
РешениеУсловие: Из предложенного перечня веществ выберите вещества, между которыми протекает реакция ионного обмена с образованием бурого осадка. Запишите молекулярное, полное и сокращённое ионные уравнения реакции.
Перечень веществ: гидроксид натрия, хлорид железа(III), серная кислота, нитрат бария, сера.
Анализ веществ: $NaOH$ — щёлочь, $FeCl_3$ — растворимая соль, $H_2SO_4$ — сильная кислота, $Ba(NO_3)_2$ — растворимая соль, $S$ — простое вещество, не электролит
Решение: Проверяем пары на образование осадка:
- $NaOH + FeCl_3$ — образуется $Fe(OH)_3\downarrow$ — нерастворимый осадок бурого цвета
- $H_2SO_4 + Ba(NO_3)_2$ — образуется $BaSO_4\downarrow$ — осадок белого цвета (не подходит)
Выбираем: $NaOH + FeCl_3$
Обратите внимание
Гидроксид железа(III) — нерастворимое основание, поэтому его не расписываем на ионы в правой части уравнения.
Задача 3. Реакция нейтрализации
РешениеУсловие: Из предложенного перечня веществ выберите кислоту и основание, между которыми протекает реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионные уравнения реакции.
Перечень веществ: азотная кислота, гидроксид калия, хлорид натрия, сульфат меди(II), железо.
Анализ веществ: $HNO_3$ — сильная кислота, $KOH$ — щёлочь, $NaCl$ — растворимая соль, $CuSO_4$ — растворимая соль, $Fe$ — металл, не электролит
Решение: По условию нужны кислота и основание:
- Кислота: $HNO_3$ (сильная, растворимая)
- Основание: $KOH$ (щёлочь)
При их взаимодействии образуется соль и вода — реакция нейтрализации.
Универсальное уравнение нейтрализации
$H^+ + OH^- = H_2O$ — это уравнение одинаково для реакций любой сильной кислоты с любой щёлочью: $HCl + NaOH$, $H_2SO_4 + KOH$, $HNO_3 + Ba(OH)_2$ и т.д.
Типичные ошибки на ЕГЭ
- Забывают проверить растворимость — всегда сверяйтесь с таблицей растворимости!
- Расписывают на ионы осадки и газы — нерастворимые вещества пишем молекулами
- Путают заряд иона и степень окисления — заряд: $Fe^{3+}$, степень окисления: $Fe^{+3}$
- Не уравнивают коэффициенты — проверяйте баланс атомов и зарядов!
- Выбирают неэлектролиты — оксиды, металлы, простые вещества не участвуют в РИО
5. Обратная задача: восстановление реакции по ионному уравнению
На экзамене иногда дают сокращённое ионное уравнение и просят подобрать реагенты. Это как работа детектива — по «уликам» (ионам) восстанавливаем «преступление» (реакцию).
Пример задачи
Дано: $3Ca^{2+} + 2PO_4^{3-} \to Ca_3(PO_4)_2\downarrow$
Решение: Наличие катиона кальция $Ca^{2+}$ и фосфат-аниона $PO_4^{3-}$ говорит о том, что реагенты — два растворимых соединения. По таблице растворимости подбираем, например: хлорид кальция и фосфат калия.
Ловушка!
Нельзя взять $Ca(OH)_2 + H_3PO_4$, так как в этом случае в ионном уравнении будут вода и слабая кислота: $3Ca(OH)_2 + 2H_3PO_4 \to Ca_3(PO_4)_2\downarrow + 6H_2O$ — это уже другое сокращённое ионное уравнение!