Гидролиз солей и среда растворов
Темы кодификатора ЕГЭ: Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная. Водородный показатель (pH). Окраска индикаторов.
1. Что такое гидролиз?
Гидролиз (от греч. hydor — вода и lysis — разложение) — это взаимодействие ионов соли с водой, приводящее к образованию слабого электролита и изменению среды раствора (pH).
Золотое правило гидролиза: «Вода разрушает СЛАБОЕ» (сильное выдерживает удар).
- Гидролиз идет по тому иону, который соответствует слабому электролиту (кислоте или основанию).
- Среду раствора определяет сильный ион (побеждает сильнейший).
2. Сила кислот и оснований
Чтобы определять тип гидролиза, нужно твердо знать, что является сильным, а что слабым.
| Основания (Катионы) | Кислоты (Анионы) |
|---|---|
|
СИЛЬНЫЕ (Щелочи) Гидроксиды активных металлов: 1. LiOH (Гидроксид лития) 2. NaOH (Едкий натр) 3. KOH (Едкое кали) 4. RbOH (Гидроксид рубидия) 5. CsOH (Гидроксид цезия) 6. Ca(OH)₂ (Гашеная известь) 7. Sr(OH)₂ (Гидроксид стронция) 8. Ba(OH)₂ (Едкий барит) |
СИЛЬНЫЕ КИСЛОТЫ (15+ примеров) 1. HCl (Соляная) 2. HBr (Бромоводородная) 3. HI (Йодоводородная) 4. HNO₃ (Азотная) 5. H₂SO₄ (Серная) 6. HClO₄ (Хлорная) 7. HClO₃ (Хлорноватая) 8. HBrO₄ (Бромная) 9. HBrO₃ (Бромноватая) 10. HIO₄ (Йодная) 11. HMnO₄ (Марганцовая) 12. H₂CrO₄ (Хромовая) 13. H₂Cr₂O₇ (Дихромовая) 14. H₂SeO₄ (Селеновая) 15. HSCN (Роданистоводородная) |
|
СЛАБЫЕ ОСНОВАНИЯ (15+ примеров) Растворимые: 1. NH₄OH (Гидрат аммиака) Нерастворимые (осадки): 2. Mg(OH)₂ (Гидроксид магния) 3. Fe(OH)₂ (Гидр. железа II) 4. Fe(OH)₃ (Гидр. железа III) 5. Cu(OH)₂ (Гидр. меди II) 6. Al(OH)₃ (Гидр. алюминия) 7. Zn(OH)₂ (Гидр. цинка) 8. Cr(OH)₃ (Гидр. хрома III) 9. Be(OH)₂ (Гидр. бериллия) 10. Mn(OH)₂ (Гидр. марганца II) 11. Ni(OH)₂ (Гидр. никеля II) 12. Co(OH)₂ (Гидр. кобальта II) 13. Pb(OH)₂ (Гидр. свинца II) 14. Sn(OH)₂ (Гидр. олова II) 15. Bi(OH)₃ (Гидр. висмута III) |
СЛАБЫЕ КИСЛОТЫ (15+ примеров) 1. HF (Плавиковая) 2. H₂S (Сероводородная) 3. HNO₂ (Азотистая) 4. H₂SO₃ (Сернистая) 5. H₂CO₃ (Угольная) 6. H₂SiO₃ (Кремниевая) 7. H₃PO₄ (Ортофосфорная) 8. HCN (Синильная) 9. HClO (Хлорноватистая) 10. HClO₂ (Хлористая) 11. HBrO (Бромноватистая) 12. HIO (Йодноватистая) 13. CH₃COOH (Уксусная) 14. HCOOH (Муравьиная) 15. H₂C₂O₄ (Щавелевая) 16. H₃BO₃ (Борная) |
3. Типы гидролиза
1. Соль: Катион СИЛЬНОГО основания + Анион СИЛЬНОЙ кислоты
Примеры: NaCl, K₂SO₄, Ba(NO₃)₂, CaCl₂ (Ca(OH)₂ — сильное).
Гидролиз: НЕ ИДЕТ.
Среда: НЕЙТРАЛЬНАЯ (pH = 7).
Слабых ионов нет, разрушать нечего.
2. Соль: Катион СЛАБОГО основания + Анион СИЛЬНОЙ кислоты
Примеры: NH₄Cl, CuSO₄, AlCl₃, Fe(NO₃)₃, MgCl₂.
Гидролиз: ПО КАТИОНУ (слабый катион).
Среда: КИСЛАЯ (pH < 7).
Объяснение: Сильная кислота "побеждает" → среда кислая.
3. Соль: Катион СИЛЬНОГО основания + Анион СЛАБОЙ кислоты
Примеры: Na₂CO₃, K₃PO₄, CH₃COONa, K₂S, LiNO₂.
Гидролиз: ПО АНИОНУ (слабый анион).
Среда: ЩЕЛОЧНАЯ (pH > 7).
Объяснение: Сильное основание "побеждает" → среда щелочная.
4. Соль: Катион СЛАБОГО основания + Анион СЛАБОЙ кислоты
Примеры: CH₃COONH₄, (NH₄)₂CO₃, Al₂S₃.
Гидролиз: И ПО КАТИОНУ, И ПО АНИОНУ (полный).
Среда: БЛИЗКА К НЕЙТРАЛЬНОЙ (зависит от констант, в ЕГЭ часто считают ≈7).
Некоторые соли (Al₂S₃, Cr₂S₃) разлагаются водой полностью с выделением газа и осадка (необратимый гидролиз).
2AlCl₃ + 3Na₂S + 6H₂O → 2Al(OH)₃↓ + 3H₂S↑ + 6NaCl
Важное исключение: Кислые соли
Обычно кислая соль дает среду, определяемую сильным компонентом, но есть нюансы:
- Сильнокислая среда: KHSO₄, NaHSO₄ (как сильная кислота).
- Слабокислая среда: NaH₂PO₄, NaHSO₃ (диссоциация H⁺ преобладает над гидролизом).
- Слабощелочная среда: NaHCO₃, K₂HPO₄, KHS (гидролиз преобладает над диссоциацией).
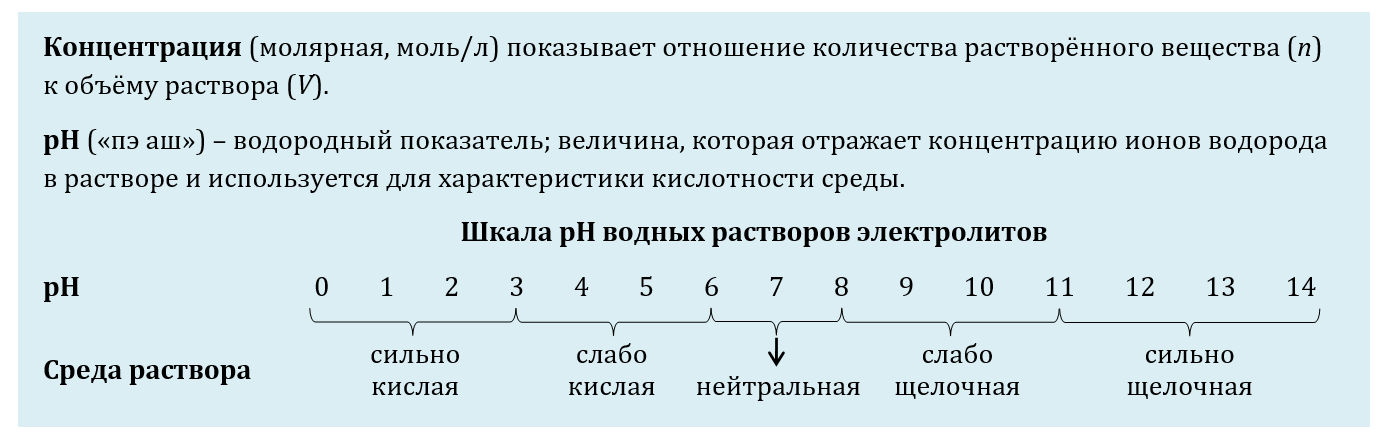
4. Среда раствора (pH)
В химии для количественной характеристики среды используют водородный показатель pH.
Нейтральная среда: чистая вода, растворы солей сильного основания и сильной кислоты.
5. Индикаторы
Вещества, меняющие цвет в зависимости от среды.
| Индикатор | В кислой среде | В нейтральной | В щелочной |
|---|---|---|---|
| Лакмус | Красный | Фиолетовый | Синий |
| Метилоранж | Розовый | Оранжевый | Желтый |
| Фенолфталеин | Бесцветный | Бесцветный | Малиновый |