Периодический закон и система химических элементов
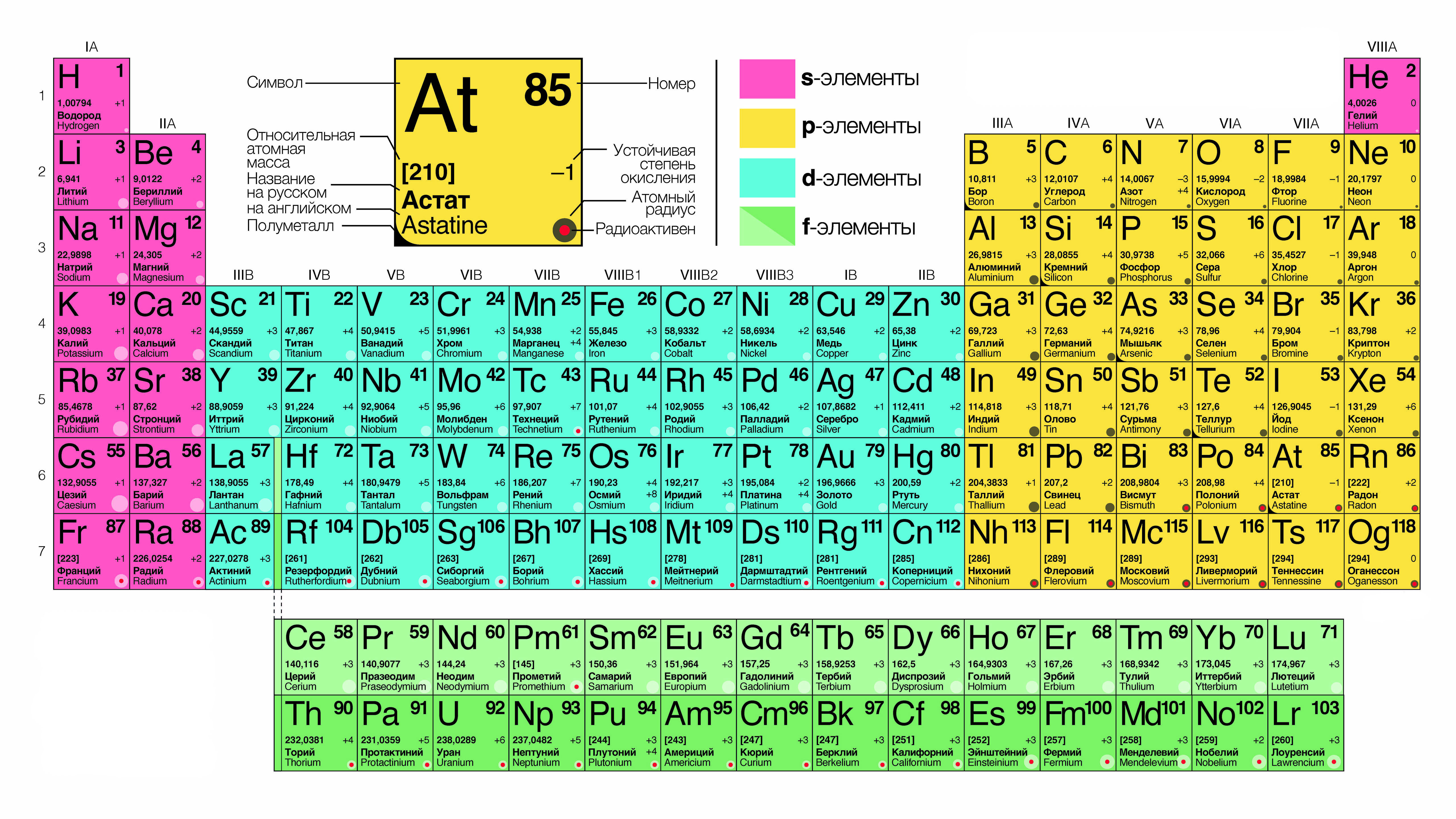
Суть закона (современная формулировка)
Свойства химических элементов, а также формы и свойства образуемых ими простых веществ и соединений находятся в периодической зависимости от величины заряда ядер их атомов.
1. Структура Периодической системы
Таблица Менделеева — это графическое отображение Периодического закона. Каждое место элемента в ней строго обосновано строением его атома.
Периоды (горизонтальные ряды)
Номер периода физически означает число энергетических уровней (электронных слоев), на которых находятся электроны. Каждый новый период начинается с заполнения нового электронного слоя (s-орбитали).
Малые периоды (1, 2, 3)
- Состоят только из одного ряда элементов.
- Происходит заполнение исключительно внешних s- и p-подуровней.
- Все элементы в этих периодах относятся к главным подгруппам.
Большие периоды (4, 5, 6, 7)
- Состоят из двух рядов (в коротком варианте таблицы).
- Включают в себя десять d-элементов (переходные металлы). У них заполняется предвнешний слой.
- В 6 и 7 периодах добавляются еще и по 14 f-элементов (лантаноиды и актиноиды).
Группы (вертикальные столбцы)
Элементы одной группы имеют сходное строение внешнего электронного слоя, поэтому проявляют похожие химические свойства. Номер группы обычно совпадает с высшей валентностью элемента.
Главная подгруппа (А)
- Содержит элементы малых и больших периодов.
- Это s- и p-элементы.
- Валентные электроны находятся на внешнем слое. Их число строго равно номеру группы.
- Например, у Галогенов (VIIA) 7 валентных электронов снаружи.
Побочная подгруппа (B)
- Содержит элементы только больших периодов.
- Это d-элементы (переходные металлы).
- Валентные электроны располагаются как на внешнем s-подуровне, так и на предвнешнем d-подуровне.
- Имеют переменные степени окисления.
Электронные семейства (блоки)
Все элементы делятся на блоки в зависимости от того, какой подуровень заполняется последним:
Блоки:
- s-элементы: IA и IIA группы, плюс H и He.
- p-элементы: С IIIA по VIIIA группу. (Почти все неметаллы).
- d-элементы: Побочные подгруппы (переходные металлы).
- f-элементы: Лантаноиды и актиноиды.
Названия главных групп:
- I A — Щелочные металлы
- II A — Щелочноземельные
- VI A — Халькогены
- VII A — Галогены
- VIII A — Инертные газы
2. Атомный и ионный радиус
Атом не имеет четкой границы, поэтому радиус — это расстояние от ядра до дальней области с высокой электронной плотностью.
Тренды изменения радиуса
| Направление | Изменение | Причина |
|---|---|---|
| По периоду (→) | Уменьшается | Число слоев неизменно, но растет заряд ядра (+). Ядро сильнее "сжимает" электронную оболочку. |
| По группе (↓) | Увеличивается | Добавляются новые электронные слои ("шубы"), атом становится крупнее. |
Сравнение радиусов частиц
Важно помнить простое правило: кто больше "минус", тот больше в размере.
Пример:
Al3+ < Mg2+ < Na+ < F- < O2-.
Это изоэлектронный ряд (у всех 10 электронов, как у неона). Выигрывает тот, у кого заряд ядра
меньше (кислород +8), так как он слабее удерживает свои электроны.
3. Электроотрицательность (ЭО)
Это мера "жадности" атома к чужим электронам. Фтор — самый "жадный" (альфа-хищник химии).
| Направление | Изменение | Причина |
|---|---|---|
| По периоду (→) | Увеличивается | Радиус уменьшается, заряд ядра растет. Ядро сильнее притягивает валентные электроны. |
| По группе (↓) | Уменьшается | Радиус атома растет, усиливается экранирование ядра внутренними слоями. |
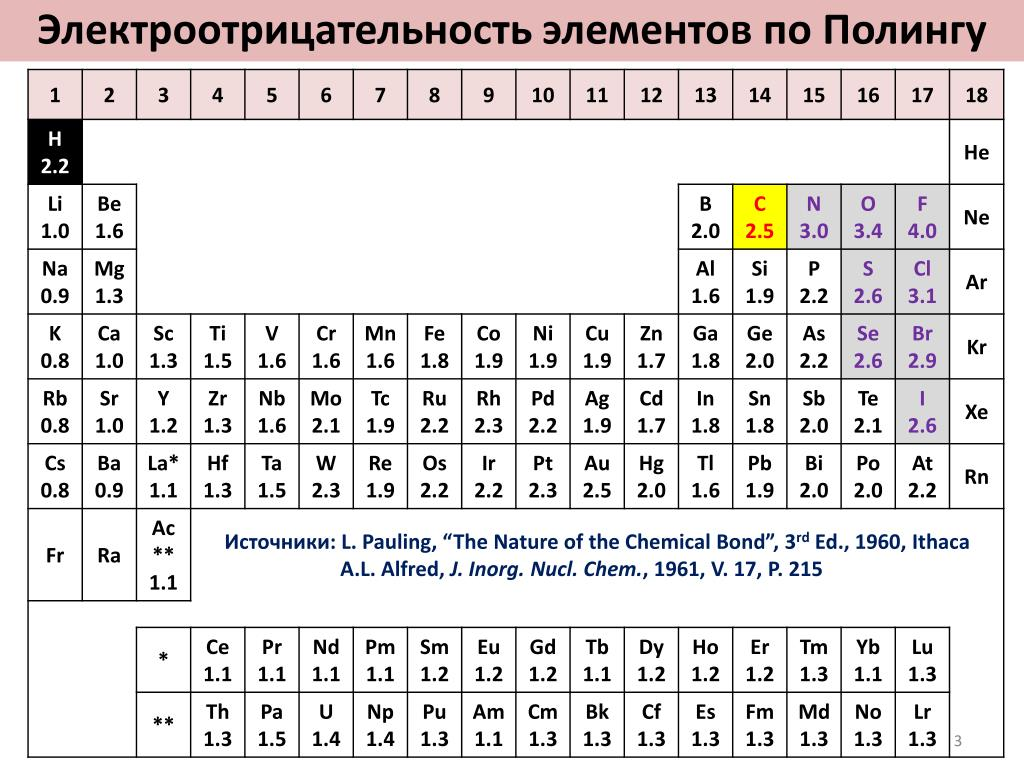
Элементы с высокой ЭО — типичные неметаллы (окислители). Элементы с низкой ЭО — металлы (восстановители).
4. Окисление и восстановление (особый фокус на ЕГЭ)
Способность отдавать или принимать электроны тесно взаимосвязана с радиусом и ЭО.
Металлические свойства (Восстановительные)
Металлические свойства — это способность атома отдавать свои внешние электроны. Чем легче он их отдает, тем он более сильный восстановитель и более активный металл. Главный (самый активный) металл в таблице — Франций (Fr).
| Направление | Изменение свойств | Главная причина |
|---|---|---|
| По периоду (→) к Фтору | Ослабевают | Радиус уменьшается, заряд ядра (плюс) растет. Электроны притягиваются так сильно, что оторвать их становится почти невозможно. |
| По группе (↓) ко Францию | Усиливаются | Радиус атома катастрофически быстро растет. Внешние электроны отдаляются от ядра и удерживаются намного слабее, отдать их очень легко. |
Неметаллические свойства (Окислительные)
Неметаллические свойства — это способность атома принимать (притягивать) чужие электроны, чтобы завершить внешний слой до устойчивого октета (8 электронов). Чем сильнее атом тянет чужие электроны, тем он более типичный неметалл. Чемпион здесь — Фтор (F).
| Направление | Изменение свойств | Главная причина |
|---|---|---|
| По периоду (→) к Фтору | Усиливаются | Радиус уменьшается, заряд ядра возрастает. Чем ближе внешний слой к ядру, тем легче ядру "зацепить" и притянуть чужой электрон. |
| По группе (↓) ко Францию | Ослабевают | Радиус атома резко растет. Из-за огромного количества оболочек, ядро уже с трудом удерживает даже свои электроны, не говоря уже о притяжении чужих. |
5. Кислотно-основные свойства соединений
Характер оксидов и гидроксидов меняется плавно. Рассмотрим общие тренды кислотных свойств:
| Направление | Кислотные свойства | Основные свойства |
|---|---|---|
| По периоду (→) | Усиливаются | Ослабевают |
| По группе (↓) | Ослабевают | Усиливаются |
Рассмотрим это на примере 3-го периода (от Na до Cl):
| Элемент | Na | Mg | Al | Si | P | S | Cl |
|---|---|---|---|---|---|---|---|
| Оксид | Na2O (осн) |
MgO (осн) |
Al2O3 (амф) |
SiO2 (кисл) |
P2O5 (kисл) |
SO3 (kисл) |
Cl2O7 (kисл) |
| Гидроксид | NaOH (щелочь) |
Mg(OH)2 (слаб. осн) |
Al(OH)3 (амфотер) |
H2SiO3 (слаб. к-та) |
H3PO4 (ср. к-та) |
H2SO4 (сильн. к-та) |
HClO4 (оч. сильн) |
Вывод: Слева направо основные свойства ослабевают, а кислотные — усиливаются.
Рассмотрим изменение свойств в главной подгруппе II группы (щелочноземельные металлы и бериллий/магний):
| Элемент | Be | Mg | Ca | Sr | Ba |
|---|---|---|---|---|---|
| Оксид | BeO (амфотер) |
MgO (осн, слаб) |
CaO (осн, щёлочь) |
SrO (осн, сильн) |
BaO (осн, оч. сильн) |
| Гидроксид | Be(OH)2 (амфотер) |
Mg(OH)2 (осн, слаб) |
Ca(OH)2 (осн, щёлочь) |
Sr(OH)2 (осн, сильн) |
Ba(OH)2 (осн, оч. сильн) |
Вывод: В группах сверху вниз основные свойства оксидов и гидроксидов усиливаются.
6. Водородные соединения
Здесь есть важная особенность. Кислотные свойства летучих водородных соединений меняются иначе, чем у кислородных кислот.
Кислотные свойства летучих водородных соединений:
| Направление | Изменение силы кислоты | Причина |
|---|---|---|
| По периоду (→) | Усиливаются | Растет полярность связи, увеличивается стабильность аниона. (CH₄ нейтр. < HF кислота). |
| По группе (↓) | Усиливаются (HF < HI) | Радиус атома растет, связь H–Э становится длиннее и слабее. H⁺ легче отщепить. |
Секрет 7-ой группы (Частая Ошибка!)
У галогенов (F, Cl, Br, I) радиус атома играет огромную роль в силе кислот. HF - слабая кислота, а HI - очень сильная. Потому что у йода радиус настолько большой, что он плохо держит протон водорода и легко отдает его в раствор (а смысл кислоты как раз в умении отдавать H⁺).