Строение атома и электронной оболочки
Темы кодификатора ЕГЭ: Строение электронных оболочек атомов элементов первых четырех периодов: s-, p- и d-элементы. Электронная конфигурация атомов и ионов. Основное и возбужденное состояние атомов.
1. История развития представлений о строении атома
Наш взгляд на микромир претерпел колоссальные изменения за последние 200 лет. Понимание эволюции этих моделей помогает лучше осознать современную квантовую теорию.
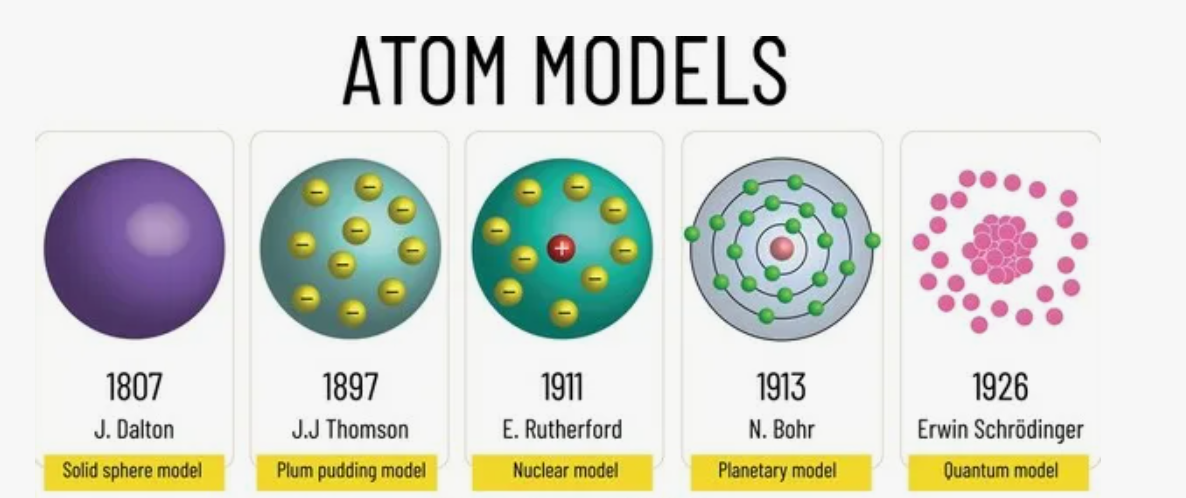
- Модель Джона Дальтона (начало XIX в.): Атом рассматривался как мельчайший, неделимый и твердый шарик. Эта теория хорошо объясняла химические реакции и закон сохранения массы, но не могла обосновать электрическую природу материи.
- Модель Дж. Дж. Томсона («Пудинг с изюмом», 1904): После открытия электрона стало ясно, что атом делим. Томсон предположил, что атом — это положительно заряженная сфера (тесто), внутри которой хаотично вкраплены отрицательные электроны (изюм), обеспечивая нейтральность.
- Планетарная модель Эрнеста Резерфорда (1911): Легендарный опыт с бомбардировкой золотой фольги альфа-частицами перевернул науку. Резерфорд доказал, что почти вся масса и весь положительный заряд сконцентрированы в крошечном ядре, а электроны вращаются вокруг него на огромных расстояниях, подобно планетам вокруг Солнца. Главной проблемой был парадокс классической физики: вращаясь, электрон должен терять энергию и упасть на ядро, но этого не происходило.
- Квантовая модель Нильса Бора (1913): Бор постулировал, что электроны могут двигаться только по строго определенным (стационарным) орбитам без излучения энергии. Переход между орбитами сопровождается поглощением или испусканием кванта энергии.
- Современная квантово-механическая модель: Отказалась от понятия траектории. Благодаря принципу неопределенности Гейзенберга мы не можем точно знать координаты и скорость электрона одновременно. Вместо орбит используется понятие орбиталь — область пространства, где вероятность нахождения электрона превышает 90%.
2. Характеристики элементарных частиц
Центральная часть атома — положительно заряженное ядро. Оно состоит из нуклонов. Количество протонов строго фиксировано для каждого элемента.
| Частица | Обозначение | Заряд (относит.) | Масса (а.е.м.) | Роль |
|---|---|---|---|---|
| Протон | p+ | +1 | ≈ 1,007 | Определяет заряд ядра и тип элемента |
| Нейтрон | n0 | 0 | ≈ 1,008 | Обеспечивает стабильность ядра, отделяет протоны |
| Электрон | e- | -1 | ≈ 1/1836 | Определяет химические свойства и объем атома |
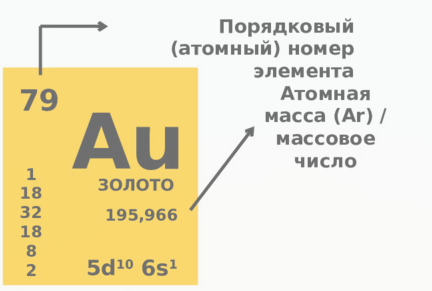
Важнейшие формулы для расчетов:
Число протонов (Z) = Порядковый номер элемента = Заряд ядра = Число электронов (в нейтральном атоме).
Массовое число (A) = Число нуклонов = Число протонов (Z) + Число нейтронов (N).
Пример: Для изотопа хлора 35Cl: p=17, e=17, n = 35 - 17 = 18.
3. Изотопы (Нуклиды)
В природе большинство элементов существует в виде смеси изотопов — атомов с одинаковым числом протонов, но разным числом нейтронов. Химические свойства изотопов идентичны, так как они зависят от строения электронной оболочки, а не от ядра. Физические свойства (например, плотность) могут незначительно отличаться.
Важные примеры:
1. Изотопы Водорода: Единственный случай, когда изотопам даны собственные названия.
- Протий (1H): 1 протон, 0 нейтронов. Основной изотоп (99.98% всего водорода Вселенной).
- Дейтерий (2H или D): 1 протон, 1 нейтрон. Стабилен. Образует D2O — тяжелую воду, используемую в ядерных реакторах.
- Тритий (3H или T): 1 протон, 2 нейтрона. Радиоактивен с периодом полураспада ~12 лет.
2. Изотопы Углерода:
- Углерод-12 (12C): Основной стабильный изотоп.
- Углерод-13 (13C): Стабильный, используется в ЯМР-спектроскопии.
- Углерод-14 (14C): Радиоактивный. Используется для радиоуглеродного датирования археологических находок.
4. Квантовые числа
Положение и состояние каждого электрона в атоме уникально и описывается набором из четырех квантовых чисел («паспорт» электрона).
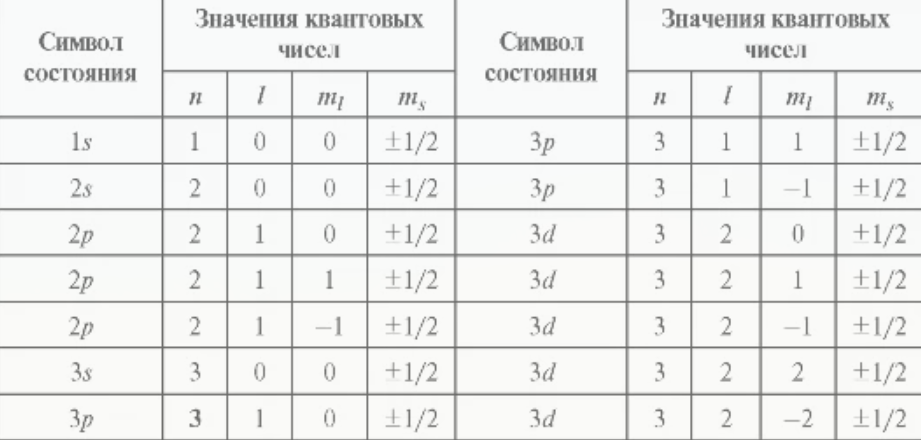
- Главное квантовое число (n): Характеризует энергию электрона и размер его орбитали. Соответствует номеру периода или электронного слоя (K, L, M, N...). Принимает целые значения от 1 до 7 (в основном состоянии). Чем больше n, тем дальше электрон от ядра.
- Орбитальное квантовое число (l): Определяет геометрическую
форму орбитали (подуровень).
- l = 0 — s-подуровень (сфера)
- l = 1 — p-подуровень (гантель)
- l = 2 — d-подуровень (клевер)
- l = 3 — f-подуровень (сложная форма)
- Магнитное квантовое число (ml): Определяет пространственную ориентацию орбитали относительно магнитного поля. Принимает целочисленные значения от -l до +l, включая ноль. Количество значений ml определяет число орбиталей на подуровне.
- Спиновое квантовое число (s): Свойство самого электрона, условно интерпретируемое как направление его вращения вокруг собственной оси. Для электрона s = ±1/2 (по часовой или против часовой стрелки).
5. Составление электронных конфигураций
Электроны в атоме стремятся занять состояние с минимальной энергией. Порядок заполнения орбиталей подчиняется Правилу Клечковского (правилу n+l):
1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → ...
Важно заметить, что 4s уровень заполняется раньше, чем 3d, так как имеет более низкую энергию (4+0=4 против 3+2=5).
Графическая формула (квантовые ячейки) показывает распределение электронов по орбиталям с учетом принципа Паули (не более 2 электронов в ячейке) и правила Хунда (сначала по одному электрону в каждую ячейку подуровня).
6. Особенности заполнения (Провал электрона)
В химии элементы подгрупп меди и хрома ведут себя "не по правилам". Это связано с особой стабильностью полностью заполненных (d10) или наполовину заполненных (d5) подуровней. Симметричное распределение заряда энергетически более выгодно атома.
Хром (Cr, №24)
Теоретически ожидалось: ...4s23d4.
Однако один электрон с 4s "проваливается" на 3d, чтобы создать стабильную конфигурацию d5.
Реально: ...4s13d5 (6 неспаренных электронов! Это объясняет высокую валентность хрома).
Медь (Cu, №29)
Теоретически ожидалось: ...4s23d9.
Один электрон переходит с 4s на 3d, завершая слой.
Реально: ...4s13d10.
Аналогичные явления наблюдаются у Молибдена (Mo), Серебра (Ag), Золота (Au).
7. Возбужденное состояние атома
Возбужденное состояние — это нестабильное состояние атома, в которое он переходит при получении энергии (нагревание, облучение). При этом электроны распариваются и переходят на свободные орбитали того же энергетического уровня.
Условие перехода: наличие свободных орбиталей на внешнем уровне и наличие спаренных электронов.
Пример: Углерод (C, №6)
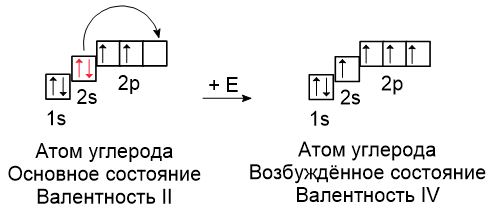
Основное состояние: 1s22s22p2.
На внешнем уровне (2-м) есть 2 распаренных электрона (на p-подуровне) и одна пустая p-орбиталь.
Валентность = II.
Возбужденное состояние (C*):
Один электрон с 2s-подуровня "перепрыгивает" на пустую 2p-орбиталь.
Конфигурация: 1s22s12p3.
Теперь 4 неспаренных электрона. Валентность = IV (именно она проявляется в органической химии,
CO2, CH4).
Пример: Азот (N, №7)
Конфигурация: 1s22s22p3. У азота на 2-м уровне нет
d-подуровня (он появляется только с 3-го уровня). Электрону с 2s некуда переходить в пределах своего
уровня. Поэтому азот не имеет возбужденного состояния с распариванием электронов и не
может быть 5-валентным.
Пример: Хлор (Cl, №17)
У хлора (3-й период) есть свободный d-подуровень, поэтому возможны переходы электронов с s- и p-подуровней на d-подуровень.
1. Основное состояние: ...3s23p5.
1 неспаренный электрон. Валентность = I (например, в HCl).
2. Первое возбужденное состояние (Cl*):
Один p-электрон переходит на d-подуровень.
...3s23p43d1. 3 неспаренных электрона. Валентность =
III (HClO2).
3. Второе возбужденное состояние (Cl**):
Еще один p-электрон переходит на d-подуровень.
...3s23p33d2. 5 неспаренных электронов. Валентность =
V (HClO3).
4. Третье возбужденное состояние (Cl***):
Один s-электрон переходит на d-подуровень.
...3s13p33d3. 7 неспаренных электронов. Валентность =
VII (HClO4).
8. Внешние и валентные электроны
Часто возникает путаница между этими понятиями. Давайте разберем их отдельно.
Внешние электроны
Это электроны, которые находятся на самом последнем (внешнем) уровне. Найти их просто: ищем в формуле самую большую цифру перед буквой (номер уровня) и считаем все электроны на этом уровне.
уровень
уровень
уровень
уровень
(сходная электронная конфигурация)
(для главных подгрупп)
Пример: Мышьяк (As, №33).
Электронная формула: [Ar] 3d10 4s2 4p3.
Самый высокий уровень — 4-й.
Электроны на 4-м уровне: 2 (на s) + 3 (на p) = 5 внешних электронов.
Валентные электроны
Это электроны, которые способны образовывать химические связи.
1. Для элементов главных подгрупп (s- и p-элементы):
Валентные электроны = Внешние электроны = Номер группы.
2. Для элементов побочных подгрупп (d-элементы):
Валентные = Внешние (s) + Предвнешние (d) (незавершенные).
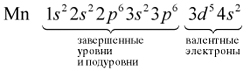
Пример: Марганец (Mn, №25).
Электронная формула: [Ar] 3d5 4s2.
Внешние: 2 (на 4s).
Валентные: 2 (4s) + 5 (3d) = 7.
9. Ионы и радиусы частиц
Ион — это заряженная частица, образующаяся при потере или приобретении электронов. Атомы стремятся приобрести конфигурацию благородного газа (октет, ns2np6) для максимальной стабильности.
Катионы (+)
Металлы отдают валентные электроны. При этом часто исчезает целый внешний электронный слой.
Na (1s22s22p63s1) - 1e → Na+ (1s22s22p6)
Радиус катиона всегда меньше радиуса исходного атома, так как уменьшается число электронных оболочек и взаимное отталкивание электронов.
Анионы (-)
Неметаллы принимают электроны до завершения слоя.
Cl (...3s23p5) + 1e → Cl- (...3s23p6)
Радиус аниона всегда больше радиуса атома, так как усиливается межэлектронное отталкивание при неизменном заряде ядра, и электронное облако "распухает".
Изоэлектронный ряд
Это ряд частиц, имеющих одинаковое количество электронов. Например, ряд с конфигурацией аргона (18e):
S2- → Cl- → Ar0 → K+ → Ca2+
заряд ядра, тем сильнее оно притягивает электроны. Поэтому радиус частиц в изоэлектронном ряду уменьшается с ростом заряда ядра.