Циклоалканы (циклопарафины, нафтены)
1. Определение и общая формула
Определение
Циклоалканы — предельные (насыщенные) углеводороды, содержащие замкнутый углеродный цикл. В молекулах присутствуют только одинарные связи C-C и C-H.
Важно
Циклоалканы имеют ту же общую формулу, что и алкены ($C_nH_{2n}$), поэтому они являются межклассовыми изомерами алкенов. Однако, в отличие от алкенов, циклоалканы не содержат кратных связей.
2. Гомологический ряд циклоалканов
| Формула | Название | T кип., °C | Агрег. сост. | Угловое напряжение |
|---|---|---|---|---|
| $C_3H_6$ | Циклопропан | -32,7 | Газ | Очень высокое |
| $C_4H_8$ | Циклобутан | 12,5 | Газ | Высокое |
| $C_5H_{10}$ | Циклопентан | 49,3 | Жидкость | Небольшое |
| $C_6H_{12}$ | Циклогексан | 80,7 | Жидкость | Отсутствует |
| $C_7H_{14}$ | Циклогептан | 118,5 | Жидкость | Отсутствует |
| $C_8H_{16}$ | Циклооктан | 149 | Жидкость | Отсутствует |
3. Строение циклоалканов
Атомы углерода в молекулах циклоалканов находятся в состоянии $sp^3$-гибридизации и образуют четыре $\sigma$-связи (C-C и C-H). Однако в зависимости от размера цикла меняются валентные углы, что приводит к угловому напряжению.
Циклопропан ($C_3H_6$)
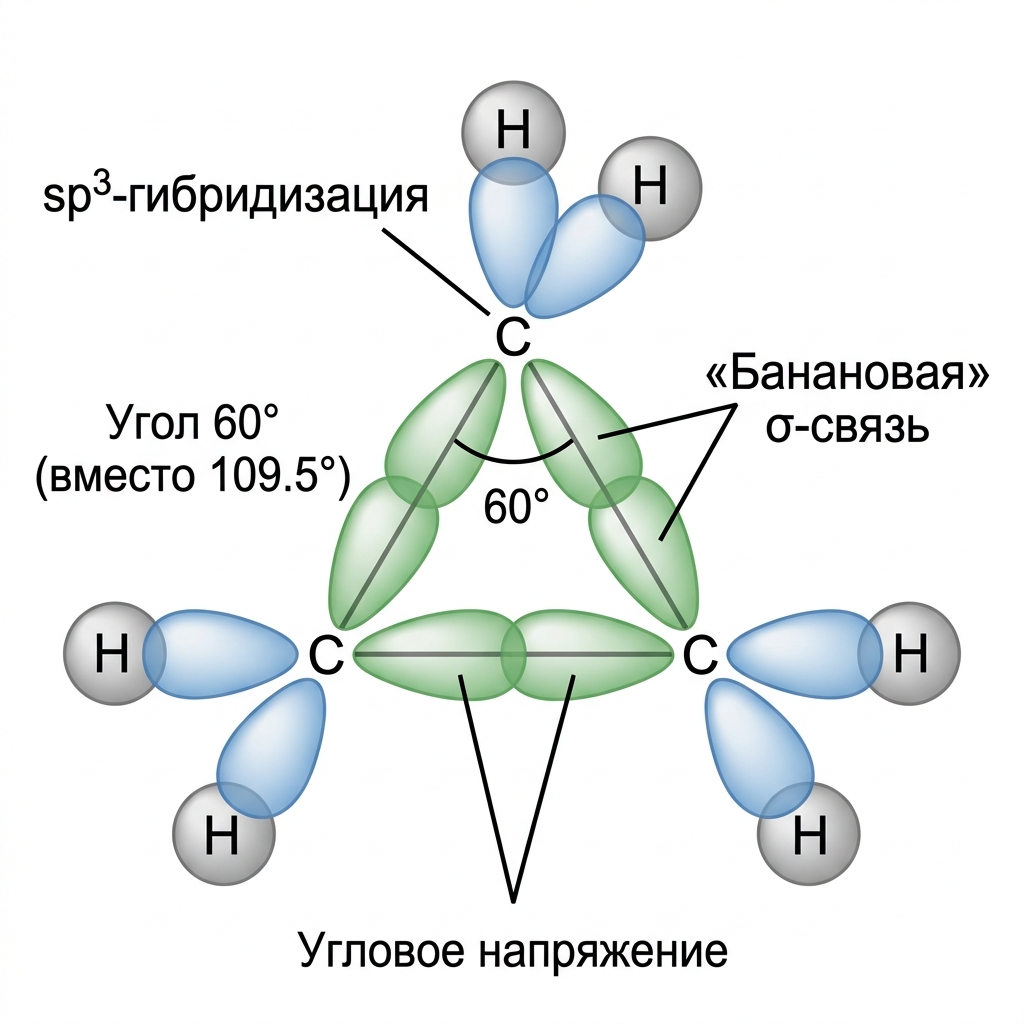
$sp^3$-гибридизация в циклопропане: «банановые» связи и угловое напряжение
Молекула циклопропана — плоский треугольник. Угол между связями C-C составляет 60°, что значительно меньше нормального тетраэдрического угла 109,5°. Это создаёт сильное угловое напряжение.
«Банановые» связи
$\sigma$-Связи в циклопропане не лежат вдоль оси, соединяющей ядра атомов C, а отклоняются от неё. По свойствам они напоминают $\pi$-связи и легко разрываются. Поэтому циклопропан вступает в реакции присоединения с разрывом цикла.
Циклобутан ($C_4H_8$)
Молекула циклобутана неплоская — имеет перегиб. Угол C-C-C ≈ 88°. Угловое напряжение меньше, чем в циклопропане, но всё ещё значительно.
Циклопентан ($C_5H_{10}$)
Молекула неплоская, принимает форму «конверта». Угловое напряжение невелико.
Циклогексан ($C_6H_{12}$)
Молекула не является плоской и принимает различные конформации. Угловое напряжение отсутствует (угол близок к тетраэдрическому).
Закономерность
Чем меньше цикл, тем больше угловое напряжение и тем легче он вступает в реакции присоединения (с разрывом кольца). Циклы из 5 и более атомов C ведут себя подобно алканам — для них характерны реакции замещения.
4. Номенклатура циклоалканов (IUPAC)
В названиях используется префикс цикло-. Алгоритм:
Примеры
5. Изомерия циклоалканов
5.1. Структурная изомерия
Для циклоалканов характерны следующие виды структурной изомерии:
Изомерия размера цикла
Различное число атомов C в кольце:
Изомерия положения заместителей
Разное расположение одинаковых заместителей в цикле:
Изомерия заместителей
Различное строение заместителей при одинаковом цикле.
5.2. Межклассовая изомерия
Важно
Циклоалканы являются межклассовыми изомерами алкенов, так как имеют одинаковую общую формулу $C_nH_{2n}$.
Например, формуле $C_3H_6$ соответствуют:
Циклопропан
Замкнутый цикл, без кратных связей. Предельный углеводород.
Пропен (пропилен)
Двойная связь C=C. Непредельный углеводород.
5.3. Геометрическая (цис-транс-) изомерия
У циклоалканов с двумя заместителями у разных атомов C в кольце возможна цис-транс-изомерия. Заместители могут находиться:
Цис-изомер
Заместители расположены по одну сторону от плоскости цикла.
Транс-изомер
Заместители расположены по разные стороны от плоскости цикла.
Внимание
Для 1,1-дизамещённых циклоалканов (оба заместителя у одного атома C) цис-транс-изомерия не характерна.
6. Физические свойства циклоалканов
- Циклопропан и циклобутан — газы
- Циклопентан и выше — жидкости или твёрдые вещества
- Нерастворимы в воде, растворимы в органических растворителях
- Температуры кипения циклоалканов выше, чем у соответствующих алканов с тем же числом атомов C
- Плотность выше, чем у алканов
7. Химические свойства циклоалканов
Химические свойства циклоалканов существенно зависят от размера цикла:
Малые циклы (C₃, C₄)
Реакции присоединения с разрывом кольца (как алкены). Высокое угловое напряжение.
Большие циклы (C₅+)
Реакции замещения без разрыва кольца (как алканы). Отсутствие углового напряжения.
7.1. Реакции малых циклов (присоединение с разрывом кольца)
Гидрирование
При нагревании в присутствии катализатора (Ni, Pt) происходит разрыв кольца с образованием алкана:
Важно
Циклопентан присоединяет водород только в жёстких условиях. Циклогексан и более крупные циклы с водородом не реагируют.
Галогенирование (присоединение)
Циклопропан и циклобутан реагируют с галогенами с разрывом цикла:
Гидрогалогенирование
Циклопропан и его гомологи реагируют с галогеноводородами с разрывом цикла:
7.2. Реакции больших циклов (замещение)
Циклопентан, циклогексан и более крупные циклы ведут себя подобно алканам.
Галогенирование (замещение)
Протекает по радикальному механизму ($S_R$) на свету или при нагревании:
Важно
При хлорировании замещённых циклоалканов замещение преимущественно идёт у третичного атома C.
Нитрование
При нагревании с разбавленной $HNO_3$:
Дегидрирование
Циклогексан и его производные при нагревании с катализатором отщепляют водород, образуя ароматические соединения:
7.3. Реакции окисления
Горение
Все циклоалканы горят с образованием $CO_2$ и $H_2O$:
Каталитическое окисление
При окислении циклогексана кислородом в присутствии катализатора образуется адипиновая кислота (гександиовая кислота) — важное промышленное сырьё для производства нейлона:
8. Способы получения циклоалканов
Алканы с 5 и более атомами C в главной цепи при нагревании с катализатором образуют циклоалканы:
При гидрировании ароматических углеводородов образуются циклогексан и его гомологи:
Этим способом получают только шестичленные циклы.
Действие активных металлов (Zn, Na) на дигалогеналканы с образованием цикла:
Этим способом можно синтезировать циклоалканы заданного строения, включая малые циклы ($C_3$, $C_4$).
Практические задания
Задача 1. Межклассовая изомерия
РешениеНапишите структурные формулы двух изомеров состава $C_4H_8$: одного циклоалкана и одного алкена.
Решение:
1) Циклобутан (циклоалкан):
2) Бутен-1 (алкен):
Также возможны: метилциклопропан, бутен-2, 2-метилпропен.
Задача 2. Реакции малых циклов
РешениеНапишите уравнения реакций циклопропана с: а) водородом; б) бромом; в) бромоводородом.
Решение:
Все реакции протекают с разрывом кольца (реакции присоединения):
а) Гидрирование:
б) Бромирование:
в) Гидрогалогенирование:
Задача 3. Реакции больших циклов
РешениеНапишите уравнения реакций циклогексана с: а) хлором (на свету); б) при дегидрировании.
Решение:
Циклогексан ведёт себя подобно алканам (реакции замещения):
а) Хлорирование (замещение, без разрыва кольца):
б) Дегидрирование:
Задача 4. Горение циклоалкана
РешениеЗапишите уравнение реакции полного сгорания циклопентана. Какой объём $CO_2$ (н.у.) образуется при сгорании 14 г циклопентана?
Решение:
Или в целых коэффициентах:
$M(C_5H_{10})$ = 70 г/моль
$n(C_5H_{10})$ = 14/70 = 0,2 моль
$n(CO_2) = 5 \times 0,2 = 1$ моль
$V(CO_2) = 1 \times 22,4 = 22,4$ л
Задача 5. Цепочка превращений
РешениеОсуществите цепочку превращений: гексан → циклогексан → бензол
Решение:
1) Дегидроциклизация гексана:
2) Дегидрирование циклогексана: