Алканы (предельные углеводороды, парафины)
1. Определение и общая формула
Определение
Алканы — предельные (насыщенные) углеводороды, в молекулах которых все атомы углерода связаны друг с другом только одинарными связями C-C и содержат максимально возможное количество атомов водорода.
Важно
Алканы относятся к классу насыщенных углеводородов, поэтому они не вступают в реакции присоединения. Для них характерны реакции замещения, разложения и окисления.
2. Гомологический ряд алканов
Все алканы — вещества, сходные по физическим и химическим свойствам и отличающиеся друг от друга на одну или несколько групп $-CH_2-$ (гомологическую разность). Такие вещества называются гомологами.
| Формула | Название | Радикал | Название радикала | T кип., °C | Агрег. сост. |
|---|---|---|---|---|---|
| $CH_4$ | Метан | $-CH_3$ | Метил | -161,5 | Газ |
| $C_2H_6$ | Этан | $-C_2H_5$ | Этил | -88,6 | Газ |
| $C_3H_8$ | Пропан | $-C_3H_7$ | Пропил | -42,1 | Газ |
| $C_4H_{10}$ | Бутан | $-C_4H_9$ | Бутил | -0,5 | Газ |
| $C_5H_{12}$ | Пентан | $-C_5H_{11}$ | Пентил (амил) | 36,1 | Жидкость |
| $C_6H_{14}$ | Гексан | $-C_6H_{13}$ | Гексил | 68,7 | Жидкость |
| $C_7H_{16}$ | Гептан | $-C_7H_{15}$ | Гептил | 98,4 | Жидкость |
| $C_8H_{18}$ | Октан | $-C_8H_{17}$ | Октил | 125,7 | Жидкость |
| $C_9H_{20}$ | Нонан | $-C_9H_{19}$ | Нонил | 150,8 | Жидкость |
| $C_{10}H_{22}$ | Декан | $-C_{10}H_{21}$ | Децил | 174,1 | Жидкость |
Важно
$C_1-C_4$ — газы, $C_5-C_{17}$ — жидкости, начиная с $C_{18}$ — твёрдые вещества. Все алканы легче воды, не растворимы в воде и не смешиваются с ней.
3. Строение алканов
В молекулах алканов встречаются два типа химических связей:
- Связь C-H — ковалентная слабополярная
- Связь C-C — ковалентная неполярная
Все связи в алканах — одинарные $\sigma$-связи.
Гибридизация
Атомы углерода в алканах находятся в состоянии $sp^3$-гибридизации. Четыре $sp^3$-гибридные орбитали направлены к вершинам тетраэдра под углом 109°28' друг к другу.
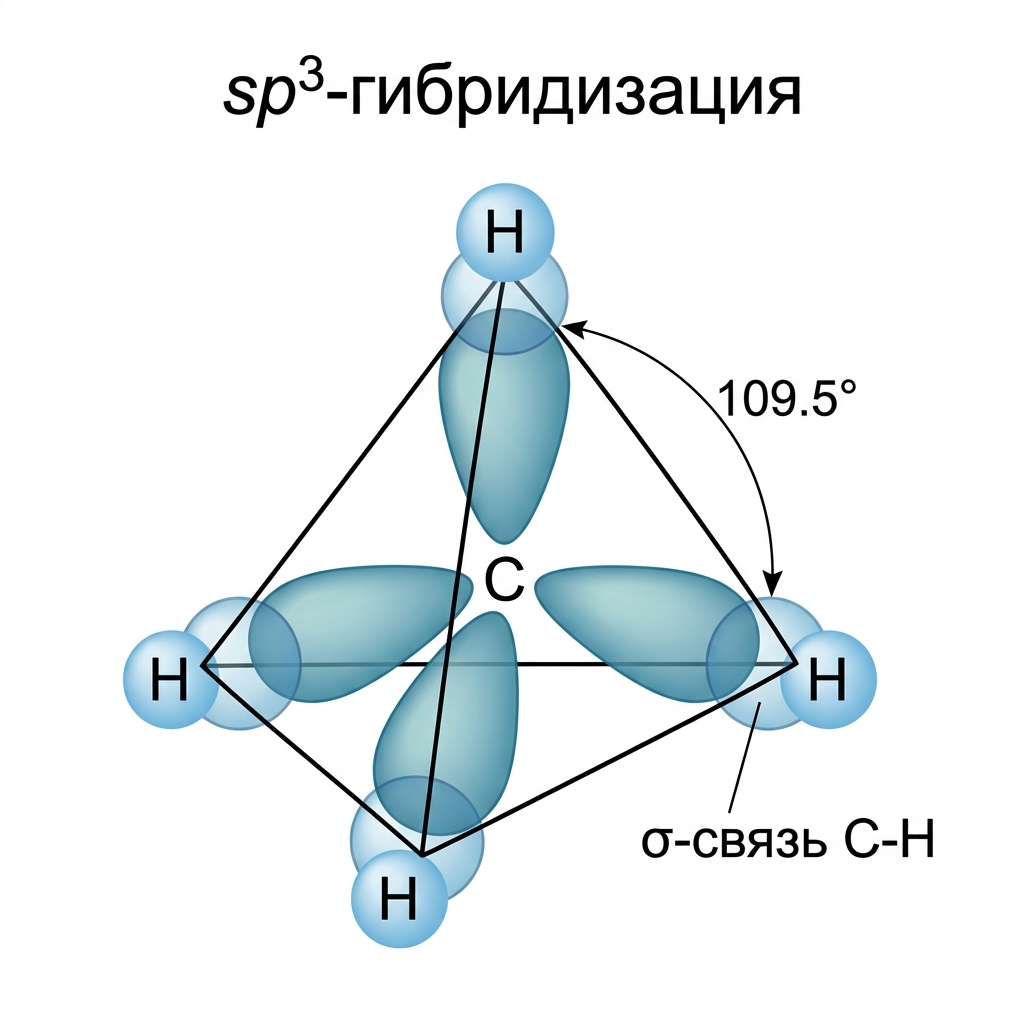
$sp^3$-гибридизация в метане ($CH_4$): тетраэдрическое расположение орбиталей
В молекуле метана $CH_4$ атомы водорода расположены в вершинах тетраэдра, в центре которого находится атом углерода. Молекулам линейных алканов с большим числом атомов углерода соответствует зигзагообразное расположение атомов C.
4. Номенклатура алканов (IUPAC)
Для названия разветвлённых алканов по систематической номенклатуре IUPAC используется следующий алгоритм:
Примеры номенклатуры
Пример 1
Главная цепь: 4 атома C (бутан). Заместитель: метил у C-2.
Название: 2-метилбутан
Пример 2
Главная цепь: 4 атома C (бутан). Два метила у C-2.
Название: 2,2-диметилбутан
Пример 3
Главная цепь: 5 атомов C (пентан). Метилы у C-2 и C-3.
Название: 2,3-диметилпентан
Пример 4
Главная цепь: 6 атомов C (гексан). Два метильных заместителя у C-3 и C-4.
Название: 3,4-диметилгексан
5. Изомерия алканов
5.1. Структурная изомерия (изомерия углеродного скелета)
Для алканов характерна изомерия углеродного скелета — изомеры отличаются строением углеродной цепи (линейная или разветвлённая).
Важно
Структурная изомерия появляется начиная с бутана ($C_4H_{10}$). Метан, этан и пропан изомеров не имеют.
Пример: формуле $C_4H_{10}$ соответствуют два изомера:
н-Бутан
Линейная цепь, T кип. = -0,5 °C
Изобутан (2-метилпропан)
Разветвлённая цепь, T кип. = -11,4 °C
Для формулы $C_5H_{12}$ существует три изомера:
С увеличением числа атомов C количество изомеров быстро возрастает:
| Формула | $C_4H_{10}$ | $C_5H_{12}$ | $C_6H_{14}$ | $C_7H_{16}$ | $C_8H_{18}$ | $C_{10}H_{22}$ |
|---|---|---|---|---|---|---|
| Число изомеров | 2 | 3 | 5 | 9 | 18 | 75 |
5.2. Оптическая изомерия
Если атом углерода в молекуле алкана связан с четырьмя различными заместителями (асимметрический атом C), возможно существование двух оптических изомеров — молекул, которые соотносятся как предмет и его зеркальное изображение.
Внимание
Для алканов не характерна изомерия положения кратной связи (нет кратных связей), геометрическая (цис-транс) изомерия, а также межклассовая изомерия (с циклоалканами — только начиная с $C_3H_6$, но циклоалканы имеют формулу $C_nH_{2n}$, отличную от алканов).
6. Физические свойства алканов
- $C_1-C_4$ — газы без цвета и запаха (метан, этан, пропан, бутан)
- $C_5-C_{17}$ — жидкости
- $C_{18}$ и выше — твёрдые вещества
- Нерастворимы в воде, растворимы в органических растворителях
- Легче воды (плотность меньше 1 г/мл)
- С ростом молекулярной массы температуры кипения и плавления возрастают
- Разветвлённые изомеры имеют более низкие температуры кипения, чем линейные
Важно
Алканы устойчивы к действию сильных окислителей ($KMnO_4$, $K_2Cr_2O_7$ и др.), не реагируют с концентрированными кислотами, щелочами, бромной водой.
7. Химические свойства алканов
Алканы — предельные углеводороды, поэтому для них характерны реакции:
Замещение
Радикальный механизм ($S_R$). Галогенирование, нитрование.
Разложение
Дегидрирование, крекинг, пиролиз метана.
Окисление
Горение, каталитическое окисление.
7.1. Реакции замещения
Разрыв слабополярных связей C-H протекает по гомолитическому (радикальному) механизму с образованием свободных радикалов.
Галогенирование
Алканы реагируют с хлором и бромом на свету (hv) или при нагревании.
Хлорирование метана (последовательное замещение):
Важно
Бромирование протекает более медленно и избирательно. Порядок легкости замещения водорода:
$C_{третичный}-H > C_{вторичный}-H > C_{первичный}-H$
Механизм радикального замещения ($S_R$)
Стадия 1. Инициирование (зарождение) цепи
Под действием света или при нагревании молекула галогена распадается на два радикала:
Стадия 2. Развитие (рост) цепи
Радикал хлора отрывает атом H от молекулы алкана, образуя алкильный радикал, который далее реагирует с молекулой $Cl_2$:
Стадия 3. Обрыв цепи
Два радикала сталкиваются и образуют молекулу:
Нитрование (реакция Коновалова)
Алканы взаимодействуют с разбавленной $HNO_3$ при нагревании до 140 °C и под давлением. Атом H замещается на нитрогруппу $-NO_2$:
Избирательность: $C_{третичный}-H > C_{вторичный}-H > C_{первичный}-H$
7.2. Реакции разложения
Дегидрирование
Отщепление атомов водорода при нагревании в присутствии катализатора (Ni, Pt, Pd, $Cr_2O_3$).
Дегидроциклизация
Алканы с 5 и более атомами C в главной цепи при дегидрировании образуют циклические соединения:
Пиролиз метана
При медленном нагревании до 1500 °C метан разлагается до простых веществ:
При быстром нагревании (~ 0,01 с) происходит межмолекулярное дегидрирование с образованием ацетилена:
Крекинг
Определение
Крекинг — реакция разложения алкана с длинной углеродной цепью на алкан + алкен с более короткой цепью.
Термический крекинг
Сильное нагревание без доступа воздуха. Образуется смесь алканов и алкенов различной длины.
Каталитический крекинг
Более низкая температура + катализатор (цеолиты). Сопровождается изомеризацией и дегидрированием.
7.3. Реакции окисления
Горение (полное окисление)
Алканы горят с образованием $CO_2$ и $H_2O$ с выделением большого количества теплоты:
Важно
При горении в недостатке кислорода может образоваться угарный газ $CO$ или сажа $C$:
$2C_3H_8 + 7O_2 \to 6CO + 8H_2O$
$CH_4 + O_2 \to C + 2H_2O$
Каталитическое окисление
Паровая конверсия метана
Окисление метана водяным паром при высокой температуре, продукт — синтез-газ:
7.4. Изомеризация
Под действием катализатора ($AlCl_3$) и при нагревании неразветвлённые алканы (от $C_4$) превращаются в разветвлённые:
8. Способы получения алканов
- Из нефти (ректификация, крекинг)
- Из природного и попутного газа
- Из каменного угля
Взаимодействие галогеналканов с металлическим натрием. Происходит удвоение углеродного скелета:
Реакция подходит для получения симметричных алканов.
Получение метана:
Сплавление солей карбоновых кислот со щелочами:
В общем виде: $R-COONa + NaOH \to R-H + Na_2CO_3$
Электролиз водных растворов солей карбоновых кислот:
Присоединение водорода к алкенам, алкинам, циклоалканам:
Из синтез-газа:
Получение метана из углерода и водорода:
Практические задания
Задача 1. Номенклатура
РешениеНазовите по систематической номенклатуре (IUPAC) следующий алкан: $CH_3-CH_2-CH(CH_3)-CH(CH_3)-CH_2-CH_3$
Решение:
- Находим самую длинную цепь: 6 атомов C (гексан)
- Нумеруем с любого конца (симметрично): C-1, C-2, C-3 (метил), C-4 (метил), C-5, C-6
- Заместители: два метила у C-3 и C-4
Задача 2. Изомеры $C_5H_{12}$
РешениеНапишите структурные формулы всех изомеров состава $C_5H_{12}$ и дайте им названия.
Решение:
Всего 3 изомера.
Задача 3. Хлорирование пропана
РешениеЗапишите уравнение реакции монохлорирования пропана. Какой основной продукт образуется при бромировании?
Решение:
При хлорировании пропана образуется смесь 1-хлорпропана и 2-хлорпропана:
При бромировании реакция протекает избирательно, основной продукт — 2-бромпропан (замещение у вторичного атома C).
Задача 4. Реакция Вюрца
РешениеКакой алкан образуется при действии натрия на 1-хлорпропан? Запишите уравнение реакции.
Решение:
Реакция Вюрца — удвоение углеродного скелета:
Образуется гексан ($C_6H_{14}$).
Задача 5. Горение алкана
РешениеЗапишите уравнение реакции полного сгорания пропана. Вычислите объем кислорода (н.у.), необходимый для сжигания 11,2 л пропана.
Решение:
По уравнению: на 1 моль пропана нужно 5 моль $O_2$.
$V(C_3H_8)$ = 11,2 л = 0,5 моль (при н.у.)
$n(O_2) = 5 \times 0,5 = 2,5$ моль
$V(O_2) = 2,5 \times 22,4 = 56$ л
Задача 6. Цепочка превращений
РешениеОсуществите цепочку превращений: $Al_4C_3 \to CH_4 \to CH_3Cl \to C_2H_6$
Решение:
1) Гидролиз карбида алюминия:
2) Хлорирование метана:
3) Реакция Вюрца: