Алкены (олефины, этиленовые углеводороды)
1. Определение и общая формула
Определение
Алкены — непредельные (ненасыщенные) нециклические углеводороды, в молекулах которых присутствует одна двойная связь C=C.
Важно
Двойная связь C=C состоит из одной $\sigma$-связи и одной $\pi$-связи. Именно $\pi$-связь определяет характерные реакции алкенов — реакции присоединения.
2. Гомологический ряд алкенов
Первый представитель ряда — этилен (этен) $C_2H_4$. Метилен $CH_2$ не существует в виде стабильной молекулы.
| Формула | Название | T кип., °C | Агрег. сост. |
|---|---|---|---|
| $C_2H_4$ | Этен (этилен) | -103,7 | Газ |
| $C_3H_6$ | Пропен (пропилен) | -47,6 | Газ |
| $C_4H_8$ | Бутен-1 | -6,3 | Газ |
| $C_5H_{10}$ | Пентен-1 | 30,0 | Жидкость |
| $C_6H_{12}$ | Гексен-1 | 63,5 | Жидкость |
| $C_7H_{14}$ | Гептен-1 | 93,6 | Жидкость |
| $C_8H_{16}$ | Октен-1 | 121,3 | Жидкость |
Важно
$C_2H_4 - C_4H_8$ — газы, начиная с $C_5$ — жидкости. Алкены не растворимы в воде, легче воды.
3. Строение алкенов
Рассмотрим строение на примере этилена $CH_2=CH_2$:
- Связь C-H — ковалентная слабополярная, одинарная ($\sigma$-связь)
- Связь C=C — двойная, ковалентная неполярная ($\sigma + \pi$)
Гибридизация
Атомы углерода при двойной связи находятся в состоянии $sp^2$-гибридизации. Три $sp^2$-гибридные орбитали расположены в одной плоскости под углом 120° друг к другу. Негибридная $p$-орбиталь перпендикулярна этой плоскости и образует $\pi$-связь.
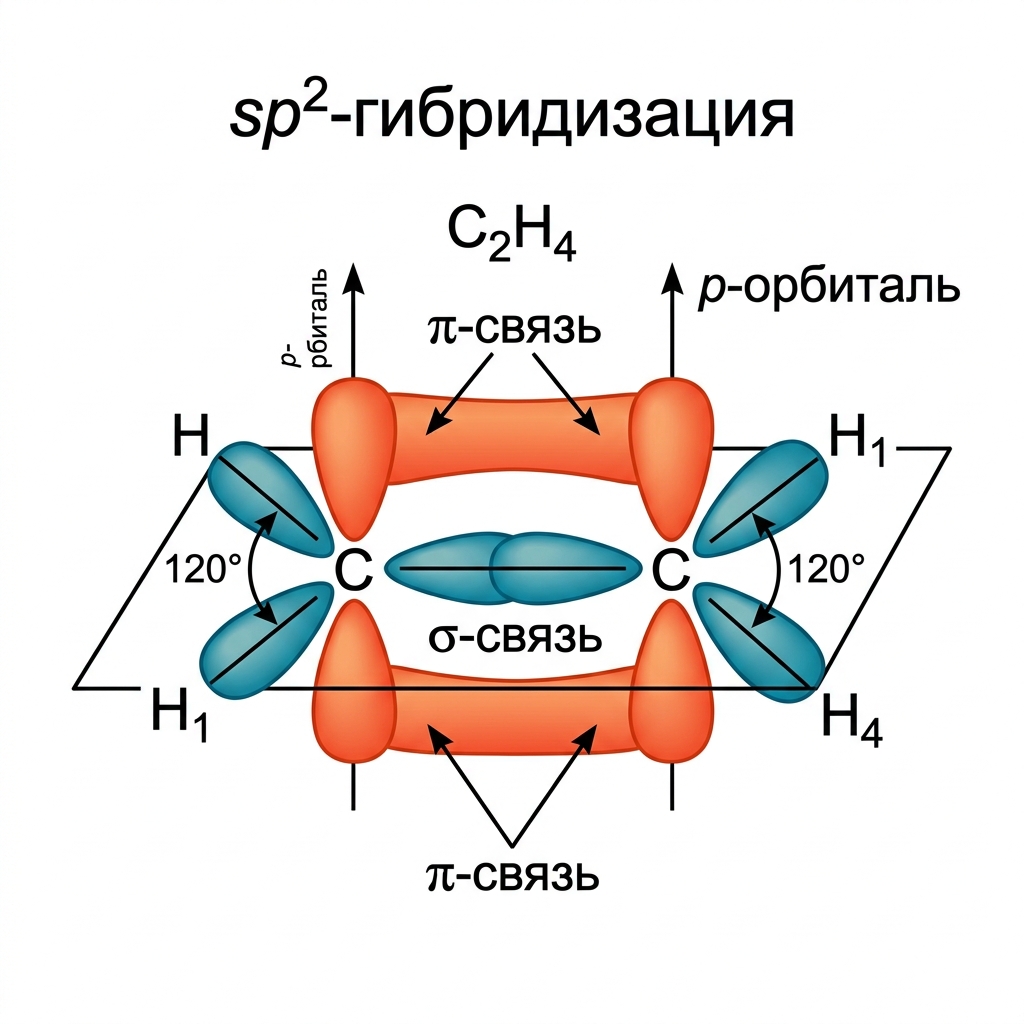
$sp^2$-гибридизация в этилене ($C_2H_4$): $\sigma$- и $\pi$-связи
$\sigma$-связь C=C
Перекрывание $sp^2$-гибридных орбиталей вдоль линии связи.
Прочная, длина 0,134 нм.
$\pi$-связь C=C
Перекрывание негибридных $p$-орбиталей над и под плоскостью молекулы.
Менее прочная, легко разрывается.
Энергия связей
$E(C=C)$ = 620 кДж/моль, $E(C-C)$ = 348 кДж/моль.
Энергия $\pi$-связи: 620 − 348 = 272 кДж/моль.
$\pi$-связь менее прочная, чем $\sigma$-связь, поэтому алкены вступают в реакции присоединения.
Важное свойство
Вращение вокруг двойной связи C=C невозможно (в отличие от одинарной C-C). Это объясняет существование цис-транс-изомеров.
4. Номенклатура алкенов (IUPAC)
Суффикс -ен (вместо -ан у алканов). Алгоритм:
Примеры
5. Изомерия алкенов
5.1. Структурная изомерия
Изомерия углеродного скелета
Различное строение углеродной цепи:
Изомерия положения двойной связи
Различное расположение C=C в цепи:
Межклассовая изомерия
Алкены изомерны циклоалканам ($C_nH_{2n}$):
5.2. Пространственная изомерия (цис-транс-)
Вращение вокруг C=C невозможно, поэтому заместители у разных атомов C при двойной связи могут располагаться по-разному:
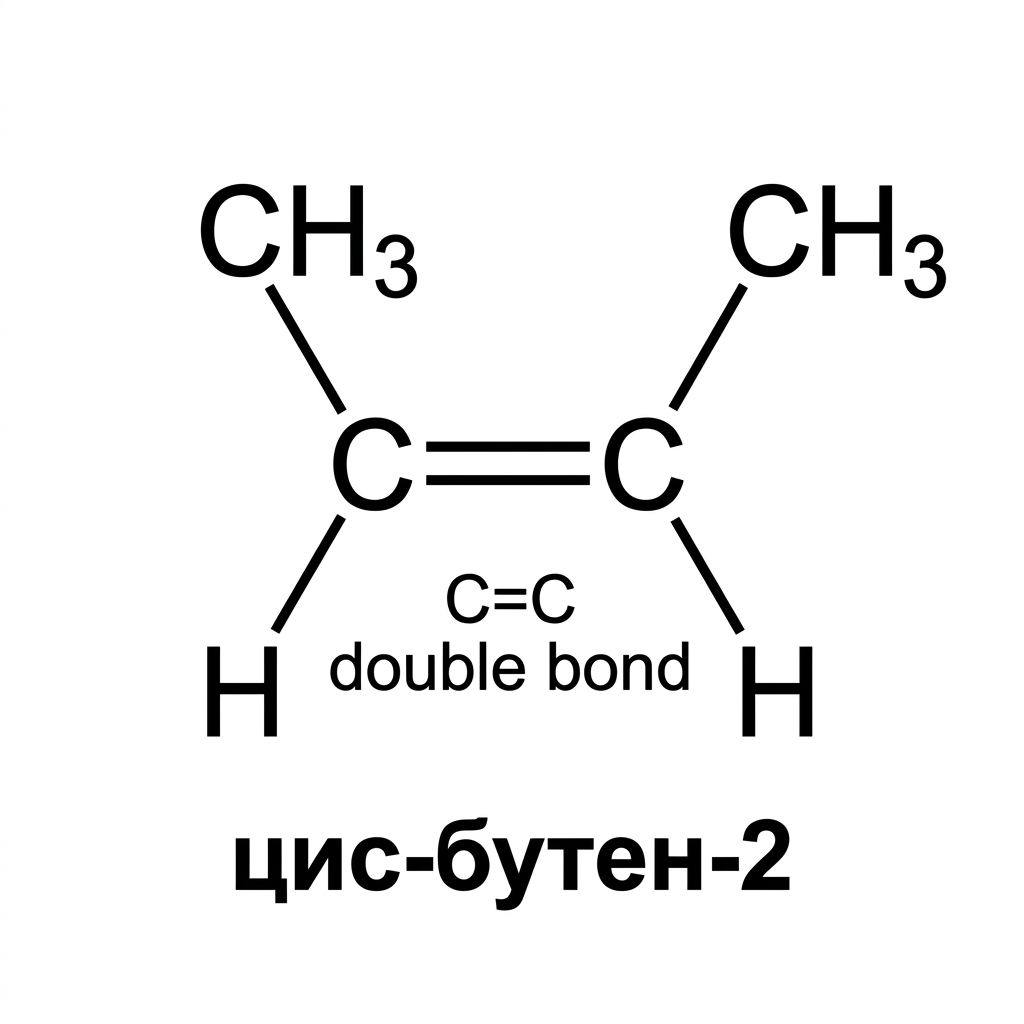
Цис-бутен-2
Группы $CH_3$ по одну сторону от плоскости C=C.
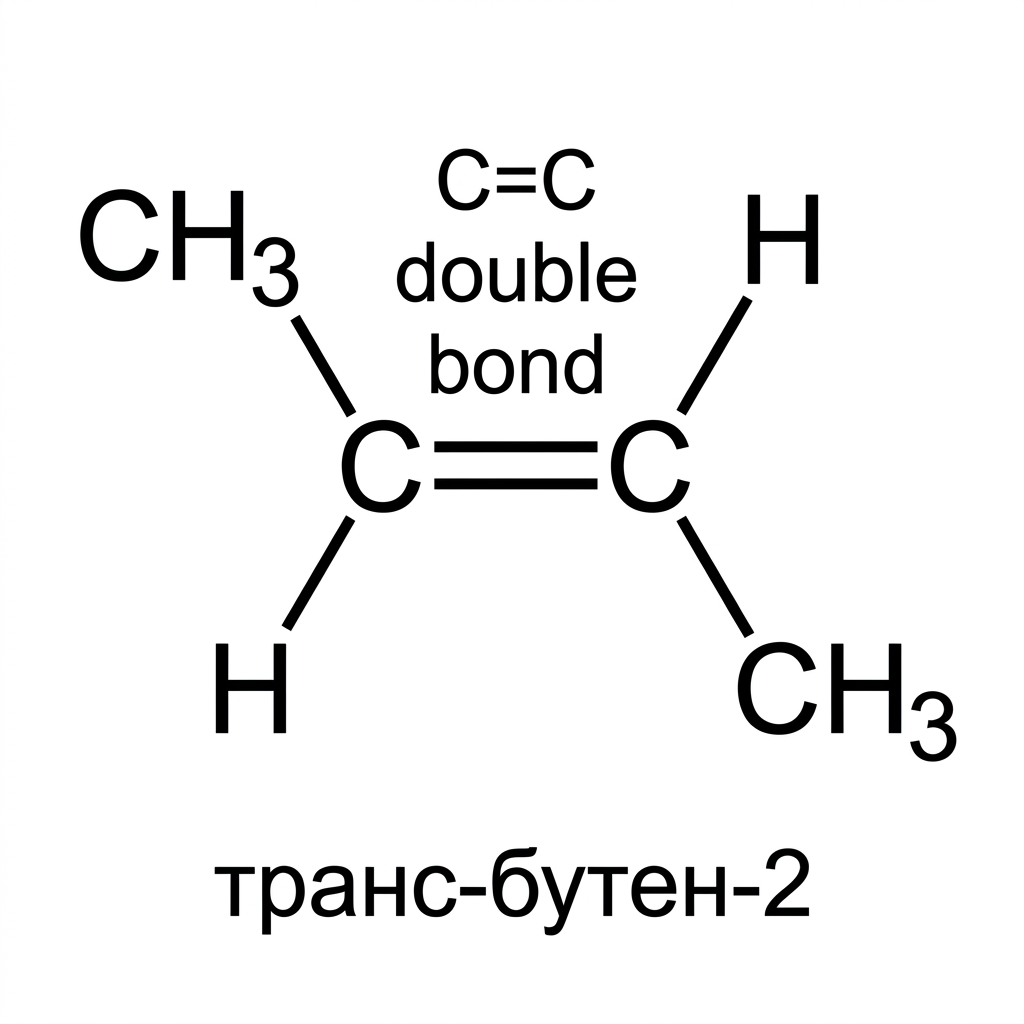
Транс-бутен-2
Группы $CH_3$ по разные стороны от плоскости C=C.
Условие цис-транс-изомерии
Цис-транс-изомерия возможна только если у каждого атома C при двойной связи два различных заместителя. Для $CH_2=CH-R$ (два одинаковых H у одного C) цис-транс-изомерия невозможна.
6. Физические свойства алкенов
- $C_2H_4 - C_4H_8$ — газы без цвета, с характерным слабым запахом
- $C_5-C_{17}$ — жидкости
- $C_{18}$ и выше — твёрдые вещества
- Нерастворимы в воде, растворимы в органических растворителях
- Легче воды
- T кипения и плавления возрастают с ростом молекулярной массы
- Цис-изомеры имеют более высокие T кипения, чем транс-изомеры
7. Химические свойства алкенов
Для алкенов характерны реакции, обусловленные разрывом $\pi$-связи:
Присоединение
$H_2$, $Hal_2$, $HHal$, $H_2O$. Разрыв $\pi$-связи.
Окисление
Горение, мягкое и жёсткое окисление.
Полимеризация
Образование высокомолекулярных соединений.
7.1. Реакции присоединения
Гидрирование
Присоединение водорода при нагревании в присутствии катализатора (Ni, Pt, Pd):
Галогенирование
Присоединение галогенов при комнатной температуре (электрофильное присоединение):
Качественная реакция!
Обесцвечивание бромной воды — качественная реакция на двойную связь C=C. Раствор $Br_2$ из бурого становится бесцветным.
Гидрогалогенирование
Присоединение галогеноводородов (HCl, HBr) — электрофильное присоединение:
Правило Марковникова
При присоединении HX к несимметричному алкену водород присоединяется к более гидрогенизированному атому углерода при двойной связи (к тому, где больше атомов H), а галоген — к менее гидрогенизированному.
Гидратация
Присоединение воды в присутствии кислот ($H_2SO_4$, $H_3PO_4$). Образуются спирты:
7.2. Реакции окисления
Горение (полное окисление)
Мягкое окисление (реакция Вагнера)
Окисление раствором $KMnO_4$ на холоду. Разрывается только $\pi$-связь, образуются двухатомные спирты (диолы):
Качественная реакция!
Обесцвечивание раствора $KMnO_4$ — вторая качественная реакция на двойную связь C=C. Фиолетовый раствор становится бесцветным (или выпадает бурый осадок $MnO_2$).
Жёсткое окисление
При действии $KMnO_4$ в кислой среде ($H_2SO_4$) или $K_2Cr_2O_7$ происходит полный разрыв двойной связи C=C. Продукты зависят от структуры алкена:
| Фрагмент при C=C | Продукт окисления |
|---|---|
| $=CH_2$ | $CO_2$ (углекислый газ) |
| $=CH-R$ | $R-COOH$ (карбоновая кислота) |
| $=CR_2$ | $R_2C=O$ (кетон) |
Каталитическое окисление этилена
7.3. Полимеризация
Определение
Полимеризация — процесс многократного соединения молекул мономера друг с другом с образованием высокомолекулярного вещества — полимера.
7.4. Замещение в боковой цепи и изомеризация
Замещение в боковой цепи
При хлорировании алкенов при нагревании до 500°C или на свету происходит не присоединение, а радикальное замещение H в аллильном положении (у C, ближайшего к C=C):
Изомеризация
При нагревании с катализатором ($Al_2O_3$) двойная связь перемещается к центру молекулы:
8. Способы получения алкенов
Протекает при высокой температуре с катализатором (Ni, Pt, Pd, $Cr_2O_3$):
Образуется наиболее замещённый алкен (с максимальным числом заместителей при C=C).
При сильном нагревании алканов происходит разрыв C-C с образованием алкана + алкен:
Отщепление воды от спиртов при нагревании с конц. $H_2SO_4$ (или $H_3PO_4$) при t > 140°C:
Правило Зайцева
Водород отщепляется от менее гидрогенизированного соседнего атома C (того, у которого меньше атомов H). Образуется более замещённый алкен.
Действие спиртового раствора щелочи на галогеналканы:
Отщепление HHal также по правилу Зайцева.
Действие металлов (Zn) на 1,2-дигалогеналканы:
Практические задания
Задача 1. Номенклатура
РешениеНазовите по IUPAC: $CH_3-CH=C(CH_3)-CH_2-CH_3$
Решение:
- Главная цепь (включает C=C): 5 атомов C (пентен)
- Нумеруем с ближнего к C=C конца: C=C между C-2 и C-3
- Заместитель: метил у C-3
Задача 2. Изомеры $C_4H_8$
РешениеНапишите структурные формулы всех изомеров-алкенов состава $C_4H_8$ и определите, для какого из них возможна цис-транс-изомерия.
Решение:
1) $CH_2=CH-CH_2-CH_3$ — бутен-1
2) $CH_3-CH=CH-CH_3$ — бутен-2
3) $CH_2=C(CH_3)-CH_3$ — 2-метилпропен
Цис-транс-изомерия возможна только для бутена-2 (у каждого C при C=C два разных заместителя: CH₃ и H).
Задача 3. Правило Марковникова
РешениеОпределите продукт реакции: $CH_3-CH=CH_2 + HCl \to ?$
Решение:
По правилу Марковникова: H присоединяется к C с бóльшим числом атомов H (к $CH_2$), а Cl — к менее гидрогенизированному C:
Задача 4. Жёсткое окисление
РешениеОпределите продукты жёсткого окисления пентена-2 ($CH_3-CH=CH-CH_2-CH_3$) раствором $KMnO_4$ в кислой среде.
Решение:
При жёстком окислении C=C полностью разрывается. Определим фрагменты:
- $CH_3-CH=$ → фрагмент $=CH-R$ → образуется $CH_3COOH$ (уксусная кислота)
- $=CH-CH_2-CH_3$ → фрагмент $=CH-R$ → образуется $CH_3CH_2COOH$ (пропионовая кислота)
Задача 5. Цепочка превращений
РешениеОсуществите цепочку: этан → этилен → этанол → этилен → 1,2-дибромэтан
Решение:
1) Дегидрирование:
2) Гидратация:
3) Дегидратация:
4) Бромирование:
Задача 6. Получение алкена
РешениеКакой алкен преимущественно образуется при дегидратации бутанола-2? Укажите правило.
Решение:
Бутанол-2: $CH_3-CH(OH)-CH_2-CH_3$
По правилу Зайцева: H отщепляется от менее гидрогенизированного соседнего C (от $CH$ у C-1, а не $CH_2$ у C-3):
Преимущественный продукт: бутен-2.