Алкины (ацетиленовые углеводороды)
1. Определение и общая формула
Определение
Алкины — непредельные (ненасыщенные) нециклические углеводороды, в молекулах которых присутствует одна тройная связь C≡C.
Межклассовая изомерия
Алкины имеют ту же общую формулу, что и алкадиены ($C_nH_{2n-2}$) и циклоалкены. Эти три класса — межклассовые изомеры.
2. Строение алкинов
Рассмотрим строение на примере ацетилена (этина) $HC \equiv CH$:
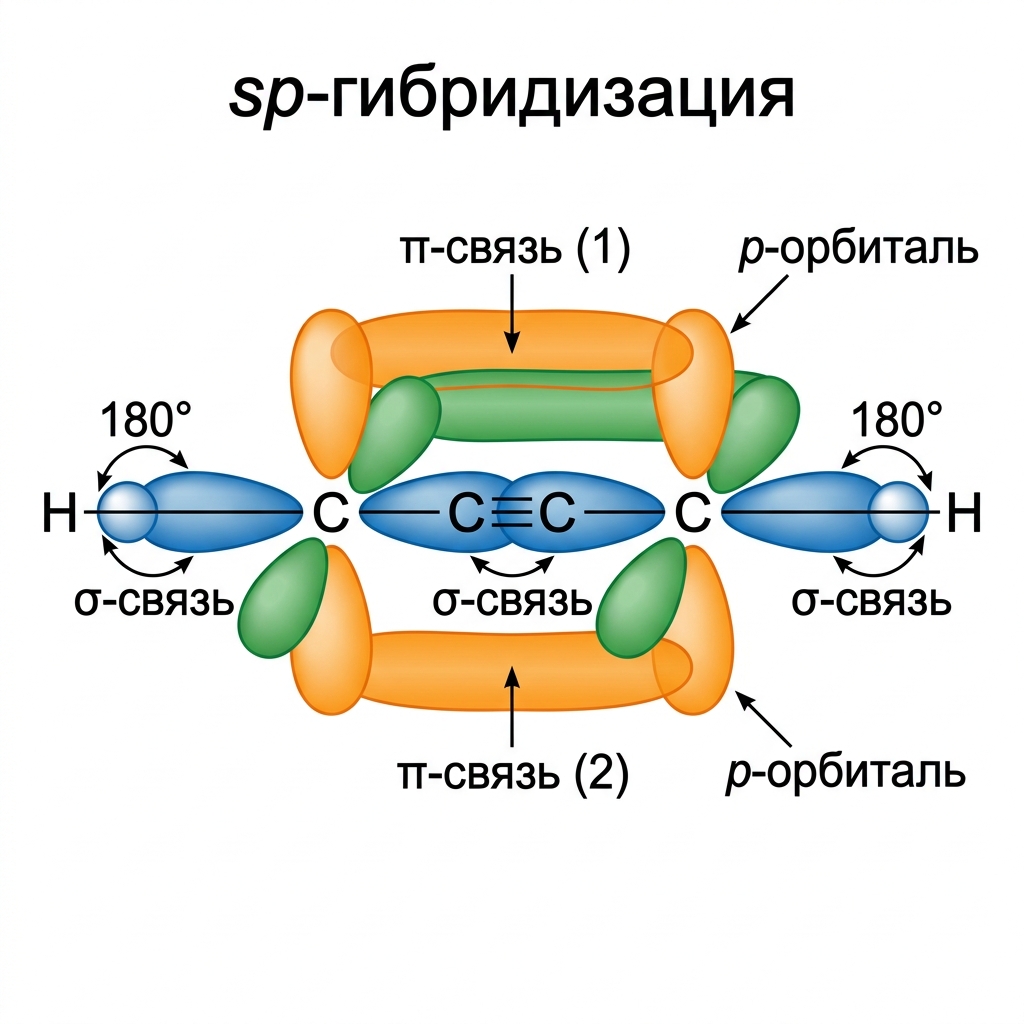
- Атомы C при тройной связи находятся в состоянии $sp$-гибридизации
- Две $sp$-гибридные орбитали расположены под углом 180° (линейная геометрия)
- Две негибридные p-орбитали на каждом C перпендикулярны друг другу и оси молекулы
- Тройная связь = 1 $\sigma$-связь + 2 $\pi$-связи
Характеристики тройной связи
Тройная связь C≡C короче (0,120 нм) и прочнее (836 кДж/моль) двойной C=C (0,134 нм, 614 кДж/моль). Однако $\pi$-электроны тройной связи менее подвижны и поляризуемы, поэтому реакции присоединения протекают сложнее, чем у алкенов.
Важно для ЕГЭ
Цис-транс-изомерия для алкинов не характерна, так как атомы при тройной связи имеют линейную геометрию.
3. Гомологический ряд алкинов
| Формула | Систематическое название | Тривиальное | T кип., °C |
|---|---|---|---|
| $C_2H_2$ | Этин | Ацетилен | -84 |
| $C_3H_4$ | Пропин | Метилацетилен | -23 |
| $C_4H_6$ | Бутин-1 | Этилацетилен | 8 |
| $C_4H_6$ | Бутин-2 | Диметилацетилен | 27 |
| $C_5H_8$ | Пентин-1 | — | 40 |
| $C_6H_{10}$ | Гексин-1 | — | 71 |
Первые два — газы, начиная с $C_5$ — жидкости, с $C_{17}$ — твёрдые.
4. Номенклатура алкинов (IUPAC)
Суффикс -ин. Правила аналогичны алкенам:
Примеры
Типы алкинов
Терминальные (концевые) алкины — тройная связь на конце цепи (R-C≡C-H). Обладают кислотными свойствами.
Внутренние алкины — тройная связь в середине цепи (R-C≡C-R'). Кислотных свойств не имеют.
5. Изомерия алкинов
5.1. Структурная изомерия
Изомерия положения тройной связи
Начиная с $C_4H_6$:
Изомерия углеродного скелета
Начиная с $C_5H_8$:
Межклассовая изомерия
Алкины $\leftrightarrow$ алкадиены $\leftrightarrow$ циклоалкены ($C_nH_{2n-2}$):
5.2. Пространственная изомерия
Запомни
Цис-транс-изомерия для алкинов не характерна! Линейная геометрия $sp$-атомов не допускает различных расположений заместителей.
6. Химические свойства алкинов
Свойства определяются тройной связью. Характерны реакции присоединения (по двум $\pi$-связям), кислотные свойства (для концевых алкинов) и окисление.
6.1. Реакции присоединения
Гидрирование
С катализатором (Ni, Pt) — последовательно через алкен до алкана:
Катализатор Линдлара
$Pd/CaCO_3$ (катализатор Линдлара) — мягкий катализатор, останавливает гидрирование на стадии алкена.
Галогенирование
Присоединение $Br_2$ — последовательно:
Гидрогалогенирование
По правилу Марковникова для несимметричных алкинов:
6.2. Реакция Кучерова (гидратация)
Реакция Кучерова
Присоединение воды к алкинам в присутствии $H_2SO_4$ и $HgSO_4$ (соли ртути II). Промежуточный продукт — енол (неустойчивый виниловый спирт), который изомеризуется в карбонильное соединение.
Правило
Из ацетилена → альдегид. Из остальных алкинов-1 → кетон (по правилу Марковникова, OH присоединяется ко 2-му C).
6.3. Ди- и тримеризация
Димеризация
Тримеризация (реакция Зелинского)
Реакция Зелинского
Тримеризация ацетилена при пропускании над активированным углём при 600°C даёт бензол. Это важнейший промышленный способ получения бензола.
6.4. Кислотные свойства (концевые алкины)
Кислотность алкинов-1
Связь ≡C-H у концевых алкинов более полярна (больше s-характер $sp$-орбитали), поэтому атом H может отщепляться как протон. Алкины-1 — слабые C-H кислоты.
Реакции с металлами
Реакция «серебряного зеркала» для алкинов (качественная!)
Качественная реакция на алкины-1
Выпадение осадка ацетиленида серебра (белый) или ацетиленида меди (I) (красный) — качественная реакция на концевую тройную связь ≡C-H.
Важно
Бутин-2 ($CH_3-C \equiv C-CH_3$) не реагирует с $[Ag(NH_3)_2]OH$ — нет концевого H при тройной связи.
6.5. Окисление
Горение
Мягкое окисление
Раствор $KMnO_4$ обесцвечивается (качественная реакция).
Жёсткое окисление
$KMnO_4$ в кислой среде — полный разрыв C≡C с образованием карбоновых кислот или $CO_2$:
7. Способы получения алкинов
Электродуговой способ при 1500°C (очень быстро, ~0,01 с):
Получение карбида кальция
$CaO + 3C \xrightarrow{t} CaC_2 + CO$
Спиртовой раствор избытка щелочи. Атомы Hal у одного или соседних C:
Ацетиленид + галогеналкан:
Практические задания
Задача 1. Изомеры $C_5H_8$
РешениеНапишите структурные формулы всех алкинов состава $C_5H_8$ и назовите их.
Решение:
1) $CH \equiv C-CH_2-CH_2-CH_3$ — пентин-1
2) $CH_3-C \equiv C-CH_2-CH_3$ — пентин-2
3) $CH \equiv C-CH(CH_3)-CH_3$ — 3-метилбутин-1
Задача 2. Реакция Кучерова
РешениеКакой продукт образуется при гидратации пропина?
Решение:
По правилу Марковникова OH присоединяется к C2 (более замещённому):
$CH_3-C \equiv CH + H_2O \xrightarrow{HgSO_4} [CH_3-C(OH)=CH_2] \to CH_3-CO-CH_3$
Задача 3. Качественная реакция
РешениеКакие из веществ: бутин-1, бутин-2, бутен-1 — реагируют с аммиачным раствором $AgNO_3$?
Решение:
С $[Ag(NH_3)_2]OH$ реагируют только концевые алкины (≡C-H).
Бутин-1 ($CH \equiv C-CH_2-CH_3$) — да, есть ≡C-H
Бутин-2 ($CH_3-C \equiv C-CH_3$) — нет, нет ≡C-H
Бутен-1 ($CH_2=CH-CH_2-CH_3$) — нет, это алкен
Задача 4. Карбидный способ
РешениеКакой объём (н.у.) ацетилена выделится при действии воды на 128 г карбида кальция ($CaC_2$)?
Решение:
$CaC_2 + 2H_2O \to Ca(OH)_2 + C_2H_2$
$M(CaC_2) = 64$ г/моль
$n(CaC_2) = 128 / 64 = 2$ моль
По уравнению: $n(C_2H_2) = n(CaC_2) = 2$ моль
$V = 2 \cdot 22{,}4 = 44{,}8$ л
Задача 5. Цепочка превращений
Решение$CaC_2 \to C_2H_2 \to C_6H_6$. Напишите уравнения реакций.
Решение:
1) Гидролиз карбида кальция:
2) Тримеризация Зелинского: