Алкадиены (диеновые углеводороды)
1. Определение и общая формула
Определение
Алкадиены — непредельные (ненасыщенные) нециклические углеводороды, в молекулах которых присутствуют две двойные связи C=C.
Межклассовая изомерия
Алкадиены имеют ту же общую формулу, что и алкины ($C_nH_{2n-2}$) и циклоалкены. Поэтому эти три класса являются межклассовыми изомерами.
2. Классификация алкадиенов по расположению C=C
Свойства алкадиенов определяются взаимным расположением двух двойных связей:
Сопряжённые Самые важные!
Двойные связи разделены одной $\sigma$-связью C-C.
бутадиен-1,3
Изолированные Как алкены
Двойные связи разделены двумя и более $\sigma$-связями.
пентадиен-1,4
Кумулированные Неустойчивы
Двойные связи у одного атома C (накопленные).
пропадиен (аллен)
Для ЕГЭ
В ЕГЭ рассматриваются преимущественно сопряжённые алкадиены (бутадиен-1,3 и изопрен). Изолированные диены ведут себя как обычные алкены, кумулированные — неустойчивы.
3. Строение сопряжённых алкадиенов
Рассмотрим строение на примере бутадиена-1,3 (дивинила) $CH_2=CH-CH=CH_2$:
- Все 4 атома C находятся в состоянии $sp^2$-гибридизации
- Молекула плоская, угол между связями ≈ 120°
- Каждый атом C имеет по одной негибридной p-орбитали, перпендикулярной плоскости молекулы
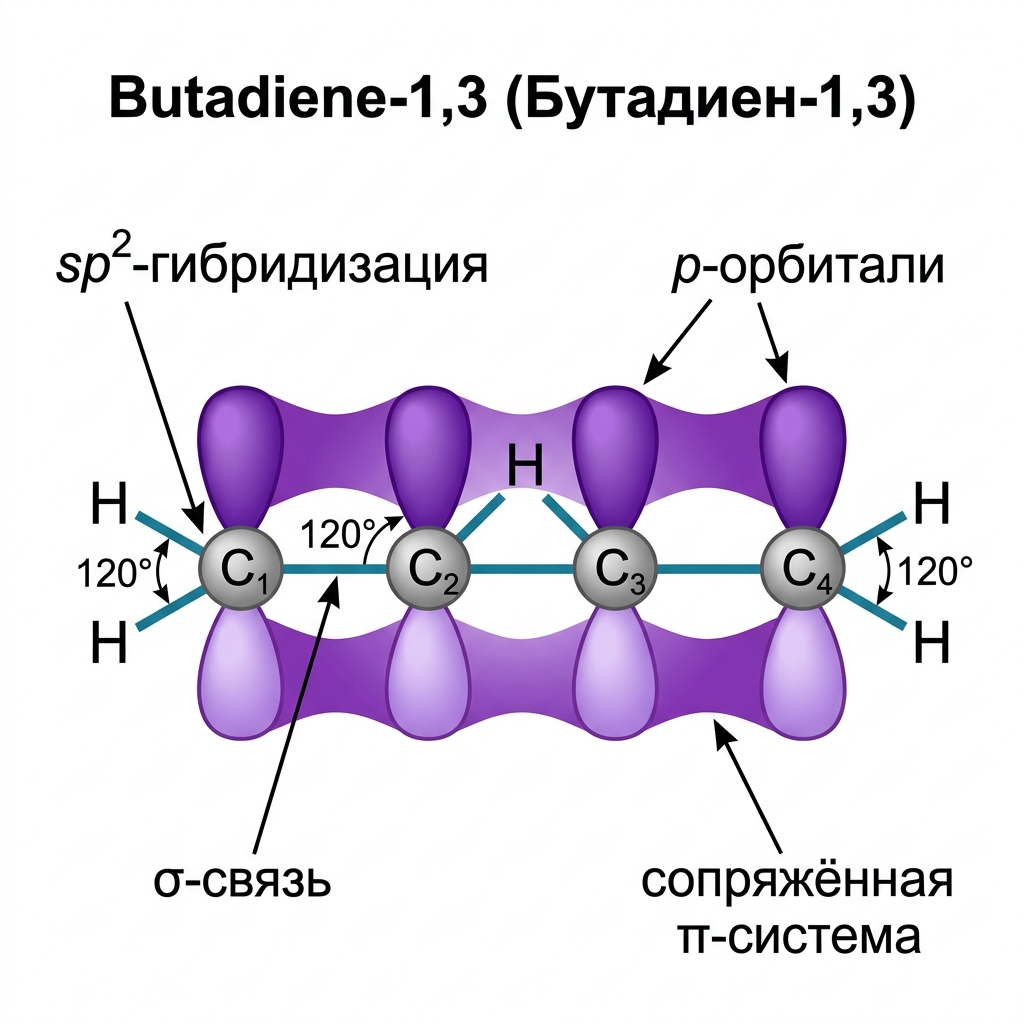
Сопряжение
$\pi$-Электроны двух двойных связей образуют единое $\pi$-электронное облако — сопряжённую систему. Электронная плотность делокализована (равномерно распределена) по всем четырём атомам C. Связь C2-C3 укорочена (0,147 нм вместо обычных 0,154 нм) и приобретает частично двойной характер.
Следствие сопряжения
Благодаря делокализации $\pi$-электронов сопряжённые диены более устойчивы, чем изолированные. Реакции присоединения могут протекать по двум направлениям: 1,2-присоединение (к одной C=C) и 1,4-присоединение (к обеим C=C с образованием новой C=C посередине).
4. Гомологический ряд сопряжённых алкадиенов
| Формула | Систематическое название | Тривиальное название | T кип., °C |
|---|---|---|---|
| $C_3H_4$ | Пропадиен-1,2 | Аллен | -34,5 |
| $C_4H_6$ | Бутадиен-1,3 | Дивинил | -4,5 |
| $C_5H_8$ | 2-Метилбутадиен-1,3 | Изопрен | 34,1 |
| $C_5H_8$ | Пентадиен-1,3 | — | 42,0 |
| $C_6H_{10}$ | Гексадиен-1,3 | — | 73,0 |
| $C_6H_{10}$ | 2,3-Диметилбутадиен-1,3 | — | 70,0 |
5. Номенклатура алкадиенов (IUPAC)
Суффикс -диен. Правила аналогичны алкенам:
Примеры
6. Изомерия алкадиенов
6.1. Структурная изомерия
Изомерия положения двойных связей
Различное расположение двух C=C в цепи:
Изомерия углеродного скелета
Различное строение углеродной цепи:
Межклассовая изомерия
Алкадиены изомерны алкинам и циклоалкенам ($C_nH_{2n-2}$):
6.2. Пространственная изомерия (цис-транс-)
Цис-транс-изомерия возможна для алкадиенов, у которых при C=C есть два различных заместителя. Для бутадиена-1,3 цис-транс-изомерия не характерна ($CH_2=$ имеет два одинаковых H).
Запомни
Для пентадиена-1,3 ($CH_2=CH-CH=CH-CH_3$) цис-транс-изомерия возможна по связи C3=C4 (разные заместители: H и CH₃).
7. Химические свойства сопряжённых алкадиенов
Химические свойства похожи на свойства алкенов: характерны реакции присоединения, полимеризации и окисления.
Два направления присоединения
При присоединении одной молекулы реагента возможны два пути:
• 1,2-присоединение — реагент присоединяется к одной C=C, вторая сохраняется.
• 1,4-присоединение — реагент присоединяется к крайним атомам C сопряжённой системы, а новая C=C образуется посередине (между C2 и C3).
7.1. Реакции присоединения
Гидрирование
С катализатором (Ni, Pt, Pd) при нагревании:
Галогенирование
Присоединение $Br_2$ при комнатной температуре:
Качественная реакция
Обесцвечивание бромной воды и раствора $KMnO_4$ — качественные реакции на алкадиены (так же, как для алкенов).
Гидрогалогенирование
Присоединение HCl к бутадиену-1,3 — преимущественно 1,4-присоединение:
7.2. Полимеризация (каучуки)
Каучуки
Полимеризация сопряжённых диенов даёт каучуки — эластичные полимеры. Полимеризация протекает преимущественно по 1,4-механизму: связи разрываются у C1 и C4, а C=C образуется между C2 и C3.
Бутадиеновый (синтетический) каучук
Изопреновый (натуральный) каучук
Вулканизация
При нагревании каучука с серой образуется резина. Атомы серы «сшивают» полимерные цепи, повышая прочность и эластичность.
7.3. Окисление
Горение
Мягкое окисление
Раствор $KMnO_4$ на холоду. Разрываются только $\pi$-связи, образуются четырёхатомные спирты (тетраолы).
Жёсткое окисление
$KMnO_4$ в кислой среде — полный разрыв обеих C=C. Продукты определяются по таблице (аналогично алкенам).
8. Способы получения алкадиенов
При высокой температуре с $Cr_2O_3$ отщепляются 2 молекулы $H_2$:
Одновременная дегидратация и дегидрирование этанола при нагревании с катализатором ($Al_2O_3 + ZnO$):
Историческая справка
Реакция Лебедева (1928 г.) позволила впервые в мире получать синтетический каучук в промышленных масштабах из дешёвого сырья — этанола.
С конц. $H_2SO_4$ при нагревании:
Действие спиртового раствора щелочи. Атомы Hal не должны быть у одного или соседних C:
Практические задания
Задача 1. Классификация
РешениеК какому типу алкадиенов (сопряжённые, изолированные, кумулированные) относятся: а) пентадиен-1,3; б) пентадиен-1,4; в) пропадиен-1,2?
Решение:
а) $CH_2=CH-CH=CH-CH_3$ — двойные связи через одну $\sigma$-связь → сопряжённый
б) $CH_2=CH-CH_2-CH=CH_2$ — двойные связи через две $\sigma$-связи → изолированный
в) $CH_2=C=CH_2$ — двойные связи у одного C → кумулированный
Задача 2. Изомеры $C_5H_8$
РешениеНапишите структурные формулы всех сопряжённых алкадиенов состава $C_5H_8$.
Решение:
1) $CH_2=CH-CH=CH-CH_3$ — пентадиен-1,3
2) $CH_3-CH=CH-CH=CH_2$ — это тот же пентадиен-1,3 (нумерация с другого конца)
3) $CH_2=C(CH_3)-CH=CH_2$ — 2-метилбутадиен-1,3 (изопрен)
Задача 3. 1,4-Присоединение
РешениеНапишите продукт 1,4-присоединения $HBr$ к бутадиену-1,3.
Решение:
При 1,4-присоединении H идёт к C1, Br — к C4, а C=C образуется между C2-C3:
Задача 4. Синтез Лебедева
РешениеКакой объём (н.у.) бутадиена-1,3 можно получить из 92 г этанола по реакции Лебедева? Выход 100%.
Решение:
$2C_2H_5OH \to CH_2=CH-CH=CH_2 + 2H_2O + H_2$
$M(C_2H_5OH) = 46$ г/моль
$n(C_2H_5OH) = 92 / 46 = 2$ моль
По уравнению: из 2 моль этанола → 1 моль бутадиена
$V = 1 \cdot 22{,}4 = 22{,}4$ л
Задача 5. Цепочка превращений
РешениеОсуществите цепочку: этанол → бутадиен-1,3 → бутадиеновый каучук
Решение:
1) Синтез Лебедева:
2) Полимеризация: