Алюминий
Химия элемента IIIA группы: самый распространенный металл
Важно для ЕГЭ
Алюминий — типичный амфотерный металл. Он сам, его оксид и гидроксид реагируют как с кислотами, так и с щелочами. В соединениях проявляет постоянную степень окисления +3.
1. Общая характеристика
Алюминий (Al) находится в III группе (главной подгруппе) 3-го периода Периодической системы. Порядковый номер 13.
Строение атома
Электронная конфигурация в основном состоянии:
В возбужденном состоянии один s-электрон переходит на p-подуровень, и конфигурация внешнего уровня становится 3s13p2, что объясняет валентность III и степень окисления +3.
Оксидная пленка
Физические свойства

Алюминий — легкий серебристо-белый металл.
- Плотность: низкая (2,7 г/см³), что делает его незаменимым в авиастроении («крылатый металл»).
- Температура плавления: 660°C.
- Проводимость: обладает высокой тепло- и электропроводностью (уступает серебру и меди, но значительно легче и дешевле их).
- Пластичность: легко поддается ковке, прокатке в фольгу и вытягиванию в проволоку.
2. Нахождение в природе
Алюминий — самый распространенный металл в земной коре (и третий элемент после кислорода и кремния). Из-за высокой активности в свободном виде не встречается.
| Название минерала | Формула / Комментарий |
|---|---|
| Боксит | Формула: Al2O3 · nH2O Комментарий: Основная руда для получения алюминия (содержит примеси SiO2,
Fe2O3). |
| Корунд | Формула: Al2O3 Комментарий: Очень твердый минерал. |
| Рубин | Формула: Al2O3 (с примесью Cr) Комментарий: Драгоценный камень красного цвета. |
| Сапфир | Формула: Al2O3 (с примесью Ti и Fe) Комментарий: Драгоценный камень синего цвета. |
| Криолит | Формула: Na3[AlF6] Комментарий: Используется как растворитель при электролизе глинозема. |
| Каолинит (Глина) | Формула: Al2O3 · 2SiO2 · 2H2O Комментарий: Основа керамики. |
| Нефелин | Формула: KNa3[AlSiO4]4 Комментарий: Важное сырье. |
3. Способы получения
Традиционное восстановление углем неэффективно из-за образования карбидов. Поэтому используется электрохимический метод.
1. Электролиз расплава оксида алюминия (Промышленный способ Холла-Эру):
Оксид алюминия (глинозем) плавится при очень высокой температуре (2050°C). Для снижения энергозатрат его растворяют в расплавленном криолите (Na3AlF6), что снижает температуру процесса до ~960°C и повышает электропроводность.
2Al2O3 электролизв криолите→ 4Al + 3O2↑
Процесс происходит с использованием графитовых электродов, которые постепенно сгорают в выделяющемся кислороде (C + O2 → CO2).
2. Химическое восстановление (Лабораторный способ):
Впервые алюминий был получен восстановлением его безводного хлорида металлическим калием (Велер, 1827):
AlCl3 + 3K t°→ Al + 3KCl
Исторический факт
4. Химические свойства алюминия
Алюминий — сильный восстановитель. В реакциях отдает 3 электрона (Al0 - 3e → Al+3).
4.1. Взаимодействие с простыми веществами
| С галогенами |
Алюминий энергично реагирует со всеми галогенами (фтор, хлор, бром, йод), образуя галогениды. Реакция с йодом начинается при добавлении капли воды, которая выступает в качестве катализатора:
2Al + 3I2 H2O→ 2AlI3
С хлором и бромом процессы часто сопровождаются воспламенением:
2Al + 3Cl2 t°→
2AlCl3
 |
| С кислородом |
Порошкообразный алюминий (или фольга) при сильном нагревании сгорает ослепительно белым пламенем. Выделяется огромное количество теплоты. Этот принцип используется в алюминиевых порошках для фейерверков:
4Al + 3O2 t°→
2Al2O3
|
| С серой |
При сплавлении порошков алюминия и серы наблюдается бурное взаимодействие с образованием сульфида. Эта соль необратимо гидролизуется (разлагается) водой:
2Al + 3S t°→
Al2S3
 |
| С углеродом |
При очень сильном нагревании (>1000°C) алюминий соединяется с углеродом, образуя карбид (метанид). При гидролизе метанида выделяется газ метан (CH4):
4Al + 3C t°→
Al4C3
|
| С азотом |
Реакция с азотом протекает значительно труднее — требуется нагревание до 800–1000°C, образуется тугоплавкий нитрид алюминия:
2Al + N2 t°→
2AlN
 |
| С фосфором |
Образуется фосфид алюминия, который под воздействием воды или влаги воздуха выделяет ядовитый газ фосфин (PH3):
Al + P t°→
AlP
|
| С водородом | Не реагирует напрямую. Гидрид алюминия (AlH3) получают косвенным путем. |
4.2. Взаимодействие со сложными веществами
| Свойство | Уравнения реакций |
|---|---|
| С водой (амальгама или без оксидной пленки) |
Если удалить защитную оксидную пленку (например, механически добавив соли ртути для образования амальгамы), алюминий активно взаимодействует с водой при обычной температуре. Выделяется водород и образуется рыхлый осадок гидроксида:
2Al + 6H2O → 2Al(OH)3↓ +
3H2↑
Обычный Al в воде не растворяется (из-за прочной плёнки Al2O3). |
| С кислотами-неокислителями (HCl, разб. H₂SO₄) |
Алюминий легко растворяется в растворах сильных кислот, вытесняя водород (так как стоит значительно левее водорода в ряду напряжений):
2Al + 6HCl → 2AlCl3 + 3H2↑
2Al + 3H2SO4(разб.) → Al2(SO4)3 + 3H2↑  |
| С конц. H₂SO₄ (при нагревании) |
На холоде концентрированная серная кислота пассивирует (не реагирует) алюминий (образуется уплотненная оксидная пленка, останавливающая реакцию). При сильном нагревании растворение происходит с выделением сернистого газа:
2Al + 6H2SO4(конц.) t°→ Al2(SO4)3
+
3SO2↑ + 6H2OВ особых условиях с конц. H2SO4 могут также выделяться S или H2S. |
| С HNO₃ (при нагревании) |
Как и с конц. серной кислотой, концентрированная HNO3 пассивирует алюминий на холоде. При нагревании образуется бурый газ (NO2). При уменьшении концентрации кислоты выделяются более глубокие продукты восстановления азота:
Концентрированная:
Al + 6HNO3(конц.) t°→
Al(NO3)3 + 3NO2↑ + 3H2O
 Разбавленная:
10Al + 36HNO3(разб.) →
10Al(NO3)3 +
3N2↑ + 18H2OОчень разбавленная:
8Al + 30HNO3(оч.разб.) →
8Al(NO3)3 +
3NH4NO3 + 9H2O
|
| С щелочами (в растворе) |
Алюминий (из-за своей амфотерности) легко реагирует с водными растворами щелочей. Разрушается оксидная пленка, выделяется водород и образуется комплексная соль (тетрагидроксоалюминат):
2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] +
3H2↑
 |
| С щелочами (в расплаве) |
При сплавлении со щелочами (без избытка воды) образуются безводные соли — алюминаты, и выделяется водород:
2Al + 2NaOH + 2H2O t°→
2NaAlO2 + 3H2↑
|
| Алюмотермия (с оксидами металлов) |
Алюминий — сильный восстановитель, применяемый для вытеснения тяжелых и тугоплавких металлов из их оксидов. Реакции идут со значительным выделением тепла и света (разгорание):
2Al + Fe2O3 t°→
Al2O3 + 2Fe
8Al + 3Fe3O4 t°→ 4Al2O3 + 9Fe 2Al + Cr2O3 t°→ Al2O3 + 2Cr |
| С окислителями в щелочной среде |
Важная особенность: в сильнощелочной среде алюминий восстанавливает нитраты и нитриты вплоть до аммиака. Реакция идет при нагревании. Водород при этом не выделяется!
8Al + 3KNO3 + 5KOH + 18H2O →
8K[Al(OH)4] + 3NH3↑
 |
Термит
5.1. Оксид алюминия (Al2O3)
Белое тугоплавкое вещество. Модификация "корунд" обладает очень высокой твердостью. Типичный амфотерный оксид.
Получение Al2O3
| Способ | Уравнение реакции |
|---|---|
| Горение металла |
Алюминий сгорает ослепительно ярко, образуя прочную кристаллическую решетку корунда:
4Al + 3O2 → 2Al2O3 |
| Разложение гидроксида |
Амфотерный гидроксид легко теряет воду при прокаливании:
2Al(OH)3 t°→
Al2O3 + 3H2O |
| Разложение нитрата |
Нитрат алюминия при термическом разложении дает оксид, диоксид азота и кислород:
4Al(NO3)3 t°→
2Al2O3 +
12NO2 + 3O2 |
Химические свойства Al2O3
| Свойство | Уравнения реакций |
|---|---|
| С водой |
Оксид алюминия (корунд) — это один из самых химически стойких оксидов. С водой он абсолютно не реагирует.
Не реагирует
|
| С кислотами (проявление основных свойств) |
Будучи амфотерным, оксид реагирует с растворами сильных кислот, образуя соли алюминия:
Al2O3 + 6HCl → 2AlCl3 +
3H2OAl2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O |
| С щелочами (проявление кислотных свойств) |
Взаимодействует с основаниями. Продукты реакции зависят от условий (наличия растворителя):
В растворе образуются растворимые комплексные соли:
Al2O3 + 2NaOH + 3H2O →
2Na[Al(OH)4]В расплаве образуются безводные соли (алюминаты):
Al2O3 + 2NaOH t°→
2NaAlO2 + H2O
|
| С основными оксидами и карбонатами |
Проявляя кислотные свойства в процессах сплавления, вытесняет более летучие кислотные оксиды (углекислый газ) или реагирует с основными оксидами:
Al2O3 + Na2O t°→ 2NaAlO2Al2O3 + Na2CO3 t°→ 2NaAlO2 + CO2↑  |
5.2. Гидроксид алюминия (Al(OH)3)
Белый студенистый осадок, нерастворимый в воде. Типичный амфотерный гидроксид.
Получение Al(OH)3
| Способ | Уравнение реакции |
|---|---|
| Действие аммиака на соль (лучший способ) |
Для получения амфотерных гидроксидов лучше всего использовать слабые основания (раствор аммиака). В избытке сильной щелочи амфотерный осадок бы растворился, а в избытке раствора аммиака — нет:
AlCl3 + 3NH3·H2O →
Al(OH)3↓ + 3NH4Cl
 |
| Недостаток щелочи + соль Al |
При осторожном добавлении щелочи (недостаток) выпадает белый осадок, который можно легко растворить дальнейшим приливанием щелочи:
AlCl3 + 3NaOH(недост.) →
Al(OH)3↓ + 3NaCl
|
| CO2 через алюминат |
При пропускании углекислого газа через раствор комплексной соли она разрушается. Образуется осадок Al(OH)3, нерастворимый в угольной кислоте:
Na[Al(OH)4] + CO2(изб) → Al(OH)3↓ +
NaHCO3
 |
| Взаимный гидролиз (соль Al³⁺ + соль слабой кислоты) |
При сливании растворов солей, образованных слабым основанием (Al3+) и слабой кислотой (карбонаты, сульфиды), происходит полный (необратимый) гидролиз:
2AlCl3 + 3Na2CO3 +
3H2O → 2Al(OH)3↓ + 3CO2↑ + 6NaCl2AlCl3 + 3Na2S + 6H2O → 2Al(OH)3↓ + 3H2S↑ + 6NaCl  |
Химические свойства Al(OH)3
| Свойство | Уравнения реакций |
|---|---|
| С кислотами (как основание) |
Легко растворяется в растворах сильных кислот с образованием солей алюминия:
Al(OH)3 + 3HCl → AlCl3 +
3H2OAl(OH)3 + 3HNO3 → Al(NO3)3 + 3H2O |
| С щелочами (как кислота) |
Свежий осадок легко растворяется в щелочах. В водном растворе образуется комплекс, а при сплавлении — алюминат:
В растворе:
Al(OH)3 + NaOH → Na[Al(OH)4]
 В расплаве:
Al(OH)3 + NaOH t°→
NaAlO2 + 2H2O
|
| Разложение (при нагревании) |
Как и все нерастворимые основания, амфотерные гидроксиды при прокаливании разлагаются:
2Al(OH)3 t°→
Al2O3 + 3H2O
|
5.3. Соли алюминия
Особенности солей
Соли алюминия и сильных кислот (хлориды, сульфаты, нитраты) растворимы в воде. Водные растворы имеют кислую среду из-за гидролиза по катиону:
Al3+ + HOH ⇄ AlOH2+ + H+
Комплексные соли (Тетрагидроксоалюминаты)
Важные для ЕГЭ реакции разрушения комплексов.
Представляйте Na[Al(OH)4] как смесь NaOH + Al(OH)3.
| Реагент | Уравнение реакции |
|---|---|
| Сильная кислота (избыток) |
Избыток сильной кислоты разрушает комплекс полностью (до соли алюминия и хлорида натрия). Осадка при этом не наблюдается:
Na[Al(OH)4] + 4HCl → NaCl + AlCl3 +
4H2O
|
| Сильная кислота (недостаток) |
При строгом добавлении кислоты в недостатке мы нейтрализуем щелочное окружение (одна из OH-групп комплекса), и выпадает Al(OH)3:
Na[Al(OH)4] + HCl → NaCl + Al(OH)3↓ +
H2O
|
| Слабые кислоты и кислотные оксиды (CO₂, SO₂, H₂S) |
Слабые кислоты способны разрушить комплекс и выделить осадок гидроксида алюминия. Сам осадок слабыми кислотами не растворяется (даже если они в избытке):
Na[Al(OH)4] + CO2 → Al(OH)3↓ +
NaHCO32Na[Al(OH)4] + H2S → 2Al(OH)3↓ + NaHS + 2H2O |
| Соли Al³⁺ |
Своеобразное сопропорционирование: комплекс отдает щелочь простому катиону. Оба продукта выпадают в виде осадка Al(OH)3:
3Na[Al(OH)4] + AlCl3 → 4Al(OH)3↓
+
3NaCl
|
| Термическое разложение |
При сильном нагревании или прокаливании комплексные соли теряют воду и превращаются в алюминаты:
Na[Al(OH)4] t°→
NaAlO2 + 2H2O
|
Алюминаты (Полученные сплавлением)
| Свойство | Уравнение реакции |
|---|---|
| С кислотами |
Алюминаты реагируют с растворами сильных кислот, растворяясь с образованием солей:
NaAlO2 + 4HCl → NaCl + AlCl3 +
2H2O
|
| Гидролиз в воде |
В водных растворах алюминаты превращаются в стабильные комплексные соединения (тетрагидроксоалюминаты):
NaAlO2 + 2H2O ⇄
Na[Al(OH)4]За счет этой реакции они создают щелочную среду. |
5.4. Бинарные соединения
Многие бинарные соединения алюминия подвергаются необратимому гидролизу.
| Соединение | Уравнения реакций |
|---|---|
| Сульфид алюминия Al2S3 |
Легко разрушается: водой (до H2S), растворами кислот и концентрированными кислотами-окислителями (окисляется вплоть до серной кислоты):
С водой:
Al2S3 + 6H2O →
2Al(OH)3↓ +
3H2S↑С кислотами:
Al2S3 + 6HCl → 2AlCl3 +
3H2S↑С конц. азотной кислотой:
Al2S3 + 30HNO3(к) →
2Al(NO3)3 + 3H2SO4 + 24NO2 +
12H2O
|
| Карбид алюминия Al4C3 |
Является метанидом (содержит C4-), поэтому при гидролизе (в присутствии воды или кислот) выделяет газ метан (CH4):
Al4C3 + 12H2O →
4Al(OH)3↓ +
3CH4↑
 |
| Нитрид алюминия AlN |
Необратимо разрушается водой (с выделением аммиака) или растворами кислот (аммиак связывается в соль аммония):
AlN + 3H2O → Al(OH)3↓ +
NH3↑AlN + 4HCl → AlCl3 + NH4Cl |
6. Качественные реакции
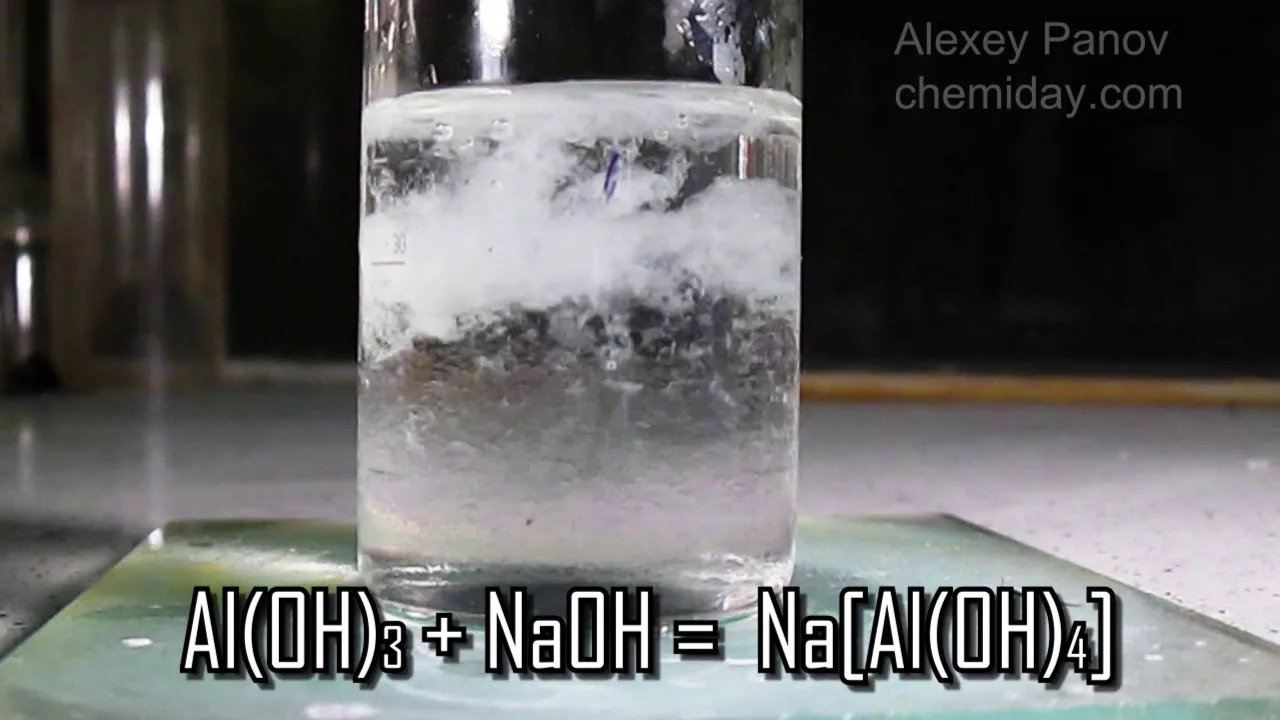
Для обнаружения иона Al3+ используют реакцию с щелочью: при постепенном добавлении щелочи сначала выпадает белый осадок, который растворяется в избытке реагента.
- Добавление OH-: Al3+ + 3OH- → Al(OH)3↓ (белый осадок)
- Избыток OH-: Al(OH)3 + OH- → [Al(OH)4]- (растворение осадка)
Если использовать раствор аммиака (NH3·H2O), осадок выпадает, но не растворяется в избытке, так как аммиак — слабое основание.
7. Видео эксперименты
Рекомендуем посмотреть опыты с алюминием на канале Thoisoi: