Щелочноземельные металлы
Химия элементов IIА группы
Важно для ЕГЭ
Щелочноземельные металлы расположены во II группе главной подгруппы (IIА). К ним традиционно относят кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Бериллий (Be) и магний (Mg) также входят в эту группу, но имеют ряд отличий. Все элементы группы проявляют постоянную степень окисления +2.
1. Общая характеристика
Элементы группы: Бериллий (Be), Магний (Mg), Кальций (Ca), Стронций (Sr), Барий (Ba), Радий (Ra).
Строение атома
Внешний электронный уровень имеет конфигурацию ns2. Два s-электрона легко отдаются в химических реакциях, поэтому металлы проявляют сильные восстановительные свойства.
Закономерности в группе (Be → Ra)
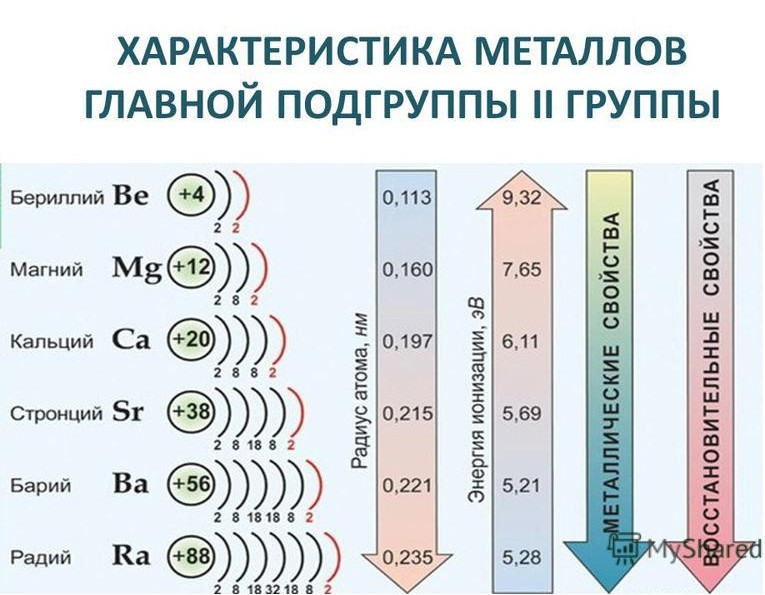
Физические свойства

Это металлы серого цвета, тверже щелочных металлов. Обладают металлической кристаллической решеткой, высокой тепло- и электропроводностью.
Хранение: Бериллий, Магний и Кальций устойчивы на сухом воздухе (покрываются оксидной пленкой). Стронций и Барий более активны, их хранят под слоем керосина.
2. Нахождение в природе
В природе встречаются исключительно в виде соединений (солей).
| Название минерала | Формула / Химическое название |
|---|---|
| Доломит | Формула: CaCO3 · MgCO3 Химическое название: Карбонат кальция-магния |
| Магнезит | Формула: MgCO3 Химическое название: Карбонат магния |
| Кальцит (Мел, Мрамор, Известняк) | Формула: CaCO3 Химическое название: Карбонат кальция |
| Гипс | Формула: CaSO4 · 2H2O Химическое название: Дигидрат сульфата кальция |
| Барит | Формула: BaSO4 Химическое название: Сульфат бария |
| Витерит | Формула: BaCO3 Химическое название: Карбонат бария |
3. Способы получения
| Способ / Металл | Описание процесса и уравнения реакций |
|---|---|
| Электролиз расплавов хлоридов (Mg, Ca, Sr) |
Основной промышленный метод получения щелочноземельных металлов. Возможен только в расплавах, так как в водных растворах на катоде выделяется водород. Для снижения температуры плавления к хлоридам добавляют другие соли (например, NaCl или KCl).
MgCl2(распл.) эл.→ Mg +
Cl2↑Магний получают электролизом расплавов обогащенного карналлита: Аналогично получают кальций электролизом расплава хлорида кальция:
CaCl2(распл.) эл.→ Ca +
Cl2↑
|
| Металлотермия / Силикотермия (Be, Mg, Ca, Ba) |
Метод восстановления металлов из их оксидов алюминотермией, магнийтермией или силикотермией. Реакции проводят при высокой температуре и часто в вакууме для отгонки паров металла.
2(CaO · MgO) + Si 1200°C→ 2Mg↑ +
Ca2SiO4Силикотермическое получение магния из обожженного доломита (смеси оксидов): Алюминотермическое получение стронция и бария в вакууме:
4BaO + 2Al 1200°C→ 3Ba↑ +
Ba(AlO2)2
|
4. Химические свойства металлов
Щелочноземельные металлы — сильные восстановители.
| Реагент | Описание процесса и уравнения реакций |
|---|---|
| С галогенами |
Регируют с парами галогенов. С бромом и йодом реакция идет при нагревании, а со фтором и хлором — уже при обычных условиях или небольшом нагревании. Образуются прочные ионные соли-галогениды:
Be + Cl2 → BeCl2
 |
| С серой и фосфором |
При нагревании активно взаимодействуют с неметаллами, образуя бинарные соединения. Фосфиды щелочноземельных металлов гидролизуются водой с выделением ядовитого газа фосфина (PH₃):
Ca + S t°→
CaS
 |
| С водородом |
Ca, Sr и Ba реагируют с водородом при нагревании с образованием гидридов (твёрдых солеобразных веществ). Магний реагирует только при повышенном давлении, а бериллий не реагирует напрямую (гидрид BeH2 получают косвенными путями):
Mg + H2 t°, p→ MgH2Ca + H2 t°→ CaH2 |
| С азотом |
Нитриды образуются при прокаливании металлов в атмосфере чистого азота или на воздухе. Полученные нитриды легко гидролизуются водой и кислотами с выделением аммиака:
3Mg + N2 t°→
Mg3N2
 |
| С углеродом |
Карбиды образуются при высоких температурах в электропечах. Важное отличие: карбид кальция — это ацетиленид (при гидролизе дает ацетилен), а карбид бериллия — метанид (при гидролизе дает метан):
Ca + 2C t°→
CaC22Be + C t°→ Be2C |
| С кислородом (Горение) |
При горении на воздухе бериллий, магний и кальций (в отличие от большинства щелочных металлов) образуют нормальные оксиды. Магний горит ослепительно белым пламенем. Из-за наличия азота в воздухе образуется смесь оксида и нитрида. Барий способен образовывать пероксид при нагревании:
2Be + O2 t°→
2BeO2Mg + O2 t°→ 2MgO Ba + O2 500°C→ BaO2 (пероксид бария) |
| С водой |
Реакционная способность с водой сильно возрастает вниз по группе от Be к Ba:
• Be не реагирует с водой даже при нагревании (защищен плотной оксидной пленкой).• Mg реагирует только с горячей водой или водяным паром с образованием малорастворимого гидроксида и водорода: Mg + 2H2O t°→ Mg(OH)2 + H2↑ • Ca, Sr, Ba бурно реагируют с выделением водорода и образованием растворимых сильных оснований (щелочей). Реакция идет уже при комнатной температуре без нагревания: Ca + 2H2O → Ca(OH)2 + H2↑ |
| С кислотами |
Щелочноземельные металлы стоят до водорода в ряду активностей. Они легко вытесняют водород из кислот-неокислителей (HCl, разб. H₂SO₄, H₃PO₄ и др.):
Mg + 2HCl → MgCl2 + H2↑
 Взаимодействие с кислотами-окислителями (H₂SO₄ конц., HNO₃):
С конц. H2SO4 возможно выделение H2S или S:Продукты зависят от концентрации кислоты и активности конкретного металла. Из-за активности этих металлов часто образуются глубокие продукты восстановления. 3Mg + 4H2SO4(конц.) → 3MgSO4 + S↓ + 4H2O  С HNO3 (продукты варьируются вплоть до N2O или нитрата аммония): 4Ca + 10HNO3(конц.) → 4Ca(NO3)2 + N2O↑ + 5H2O 4Ba + 10HNO3(оч.разб.) → 4Ba(NO3)2 + NH4NO3 + 3H2O  |
| Восстановление оксидов | Могут восстанавливать неметаллы (Si, C, B) из их оксидов. 2Ca + SiO2 → 2CaO + Si Магний горит в углекислом газе (в сухом льде): 2Mg + CO2 → 2MgO + C  |
| Вытеснение металлов | В расплавах и даже в твердых смесях (при поджигании) вытесняют менее активные металлы. Ca + CuCl2(расплав) → CaCl2 + Cu Mg + 2AgNO3 → Mg(NO3)2 + 2Ag |
5.1. Оксиды (MO)
Оксиды Ca, Sr, Ba, Mg — основные. Оксид бериллия BeO — амфотерный.
Получение:
| Способ / Условие | Описание процесса и уравнения реакций |
|---|---|
| Окисление металлов |
Щелочноземельные металлы сгорают в кислороде с образованием оксидов (барий частично образует пероксид):
2Ca + O2 → 2CaO |
| Разложение карбонатов |
Оксиды щелочноземельных металлов получают прокаливанием природных карбонатов — минералов известняка, доломита, магнезита:
CaCO3 t°→ CaO +
CO2MgCO3 t°→ MgO + CO2 |
| Разложение нитратов |
Оксиды можно получить сильным прокаливанием нитратов:
2Ca(NO3)2 t°→ 2CaO + 4NO2 +
O2 |
| Разложение гидроксидов |
Нерастворимые (Be, Mg) и слаборастворимые (Ca) гидроксиды разлагаются при нагревании:
Mg(OH)2 t°→ MgO +
H2O |
Химические свойства:
| Реагент / Условие | Описание процесса и уравнения реакций |
|---|---|
| С кислотными оксидами |
Основные оксиды реагируют с кислотными с образованием солей:
MgO + CO2 → MgCO3 |
| С кислотами |
Взаимодействуют с кислотами с образованием соли и воды:
CaO + 2HCl → CaCl2 + H2O |
| С водой |
Наиболее активные оксиды реагируют с водой, образуя щелочи («гашение извести»):
CaO, SrO, BaO реагируют активно:
CaO + H2O → Ca(OH)2
 MgO реагирует только при нагревании:
MgO + H2O t°→
Mg(OH)2BeO с водой не реагирует.
|
| Свойства амфотерного BeO |
Оксид бериллия проявляет не только основные, но и кислотные свойства (реакции с щелочами и основными оксидами):
С основными оксидами:BeO + Na2O t°→ Na2BeO2 (бериллат натрия) Со щелочами (при сплавлении) образуются безводные бериллаты: BeO + 2NaOH t°→ Na2BeO2 + H2O С растворами щелочей образует комплексные соли (тетрагидроксобериллаты): BeO + 2NaOH + H2O → Na2[Be(OH)4] |
5.2. Гидроксиды (M(OH)2)
Гидроксиды Ca, Sr, Ba — щелочи (сила основания растет от Ca к Ba). Mg(OH)2 — нерастворимое основание. Be(OH)2 — амфотерный гидроксид.
Получение:
| Способ / Реагент | Описание процесса и уравнения реакций |
|---|---|
| Оксид + Вода |
Для оксидов кальция, стронция и бария реакция с водой носит экзотермический характер и приводит к образованию щелочей. Процесс "гашения извести" (превращение CaO в Ca(OH)₂):
CaO + H2O → Ca(OH)2
|
| Металл + Вода |
Реакция простых веществ (от Ca до Ba) с водой идет бурно, вытесняя водород и образуя сильные растворимые основания:
2Ca + 2H2O → 2Ca(OH)2 +
H2↑ |
| Обменная реакция |
Известно, что гидроксиды магния и кальция малорастворимы. Их можно осадить из растворов солей добавлением избытка более сильной щелочи (NaOH или KOH):
Ca(NO3)2 + 2KOH → Ca(OH)2↓ +
2KNO3
|
Химические свойства:
| Реагент / Свойство | Описание процесса и уравнения реакций |
|---|---|
| С кислотами |
Реакция нейтрализации: основания взаимодействуют с кислотами с образованием соли и воды. Гидроксиды Ca, Sr, Ba являются сильными основаниями и реагируют с любыми кислотами. Гидроксид магния — нерастворимое основание, он взаимодействует преимущественно с сильными кислотами:
Ca(OH)2 + 2HCl → CaCl2 +
2H2OMg(OH)2 + H2SO4 → MgSO4 + 2H2O |
| С кислотными оксидами |
Растворимые гидроксиды реагируют с кислотными оксидами. Если гидроксид в избытке, образуется средняя соль. Если кислотный оксид в избытке (или пропускается долго) — образуется кислая соль (гидрокарбонаты, гидросульфиты, гидрофосфаты):
Ba(OH)2(изб.) + CO2 → BaCO3↓ +
H2O (средняя соль)
 |
| С амфотерными оксидами и гидроксидами (для Ca, Sr, Ba) |
В расплаве (образуются средние соли): Ba(OH)2 + Al2O3 t°→ Ba(AlO2)2 + H2O В растворе (образуются комплексные соли): Ba(OH)2 + Al2O3 + 3H2O → Ba[Al(OH)4]2 |
| С кислыми солями |
Добавление щелочи к кислой соли вызывает ее "донейтрализацию", отщепляя остаточный протон. При этом в случае кальция выпадает осадок нерастворимого среднего карбоната:
Ca(OH)2 + Ca(HCO3)2 →
2CaCO3↓ + 2H2O
 |
| С неметаллами |
Основания щелочноземельных металлов могут реагировать с простыми неметаллами в реакциях диспропорционирования (зависит от t°). Хлор, бром, йод, сера и фосфор взаимодействуют с образованием смеси солей:
|
| С амфотерными металлами (Be, Al, Zn) |
Щелочи растворяют металлы, оксиды которых обладают амфотерными свойствами. При этом выделяется водород и образуется комплексная соль:
В расплаве:Ca(OH)2 + Zn t°→ CaZnO2 + H2↑ В растворе: Ca(OH)2 + 2Al + 6H2O → Ca[Al(OH)4]2 + 3H2↑ |
| Обменные реакции с солями |
Щелочи вступают в реакции ионного обмена с солями, если продуктом является осадок нерастворимого гидроксида/соли или выделяется газ (как аммиак при реакции с солями аммония):
Ba(OH)2 + FeCl2 → BaCl2 +
Fe(OH)2↓2NH4Br + Ca(OH)2 → CaBr2 + 2NH3↑ + 2H2O |
| Термическое разложение |
В отличие от щелочей натрия и калия, большинство гидроксидов элементов II группы (кроме Ba(OH)₂) обладают достаточно низкой термической стабильностью и полностью разлагаются на оксид и воду при прокаливании:
Mg(OH)2 t°→ MgO +
H2O
|
| Сила оснований |
По группе вниз сила оснований увеличивается: Mg(OH)₂ — слабое основание, Ca(OH)₂ — щелочь средней силы, а Ba(OH)₂ — сильная щелочь:
Ba(OH)2 ⇄ Ba2+ +
2OH-Mg(OH)2 — нерастворимое основание. Be(OH)2 — амфотерный
гидроксид.
|
| Свойства амфотерного Be(OH)2 |
Гидроксид бериллия (как и оксид) способен проявлять кислотные свойства в реакциях с сильными щелочами, образуя гидроксокомплексы в водном растворе и безводные соли при сплавлении:
В расплаве:Be(OH)2 + 2NaOH t°→ Na2BeO2 + 2H2O В растворе: Be(OH)2 + 2NaOH → Na2[Be(OH)4] |
5.3. Соли и жесткость воды
Разложение нитратов
| Соль / Условие | Описание процесса и уравнения реакций |
|---|---|
| Термическое разложение |
Нитраты щелочноземельных металлов при прокаливании разлагаются до нитритов и кислорода, однако при более сильном нагреве нитриты распадаются до оксидов. Нитрат магния разлагается напрямую до оксида, диоксида азота и кислорода:
Ca(NO3)2 t°→
Ca(NO2)2 + O2↑

Примечание: В некоторых условиях или источниках указывается
разложение до оксида (как при получении оксидов).
|
Карбонаты
| Свойство / Реагент | Описание процесса и уравнения реакций |
|---|---|
| Термическое разложение |
Карбонаты щелочноземельных металлов, а также магния разлагаются при сильном нагревании на оксид металла и углекислый газ. Обжиг известняка (CaCO₃) — основной промышленный способ получения негашеной извести:
CaCO3 1000°C→
CaO + CO2
|
| С сильными кислотами |
Карбонаты растворяются в кислотах, более сильных чем угольная, с выделением углекислого газа:
CaCO3 + 2HCl → CaCl2 + CO2↑ +
H2O
|
| Превращение в гидрокарбонаты (растворение осадка) |
При длительном пропускании углекислого газа через водную суспензию нерастворимого карбоната образуется растворимая кислая соль — гидрокарбонат:
CaCO3 + H2O + CO2(изб) →
Ca(HCO3)2
|
| Сплавление с менее летучими оксидами (SiO2, Al2O3) |
В процессах сплавления более массивные и нелетучие кислотные (или амфотерные) оксиды с легкостью вытесняют летучий углекислый газ из карбонатов:
CaCO3 + Al2O3 t°→ Ca(AlO2)2 +
CO2↑ |
Жесткость воды
Обусловлена наличием солей кальция и магния.
Временная (карбонатная) жесткость: Гидрокарбонаты Ca(HCO3)2 и Mg(HCO3)2.
Постоянная (некарбонатная) жесткость: Хлориды и сульфаты (CaCl2, MgSO4 и др.).
Способы устранения:
| Способ (Реагент) | Описание процесса и уравнения реакций |
|---|---|
| Кипячение (только для временной) |
При кипячении гидрокарбонаты кальция и магния разрушаются, образуя нерастворимые карбонаты (накипь), которые выпадают в осадок, умягчая воду:
Ca(HCO3)2 t°→ CaCO3↓ + CO2↑ +
H2O |
| Добавление извести Ca(OH)2 (для временной) |
Известковое молоко связывает избыточную углекислоту в гидрокарбонатах, переводя их в нерастворимые средние соли:
Ca(HCO3)2 + Ca(OH)2 →
2CaCO3↓ + 2H2O |
| Добавление соды Na2CO3 (для постоянной) |
Сода осаждает растворимые хлориды и сульфаты кальция и магния в виде нерастворимых карбонатов:
CaCl2 + Na2CO3 →
CaCO3↓ + 2NaCl |
| Добавление фосфатов Na3PO4 (для постоянной) |
Ортофосфаты образуют крайне нерастворимые соединения с кальцием и магнием, полно удаляя их из раствора:
3CaCl2 + 2Na3PO4 →
Ca3(PO4)2↓ + 6NaCl |
6. Качественные реакции
Окрашивание пламени
- Кальций (Ca2+): Кирпично-красный цвет
- Стронций (Sr2+): Карминово-красный (алый)
- Барий (Ba2+): Яблочно-зеленый

Осаждение ионов
- На ионы Mg2+: Взаимодействие с щелочами (белый осадок):
Mg2+ + 2OH- → Mg(OH)2↓
- На ионы Ca2+, Sr2+, Ba2+: Взаимодействие с
карбонатами (белый осадок):
Ca2+ + CO32- → CaCO3↓
Ba2+ + CO32- → BaCO3↓ - На ионы Sr2+, Ba2+: Взаимодействие с сульфатами (белый
осадок):
Ba2+ + SO42- → BaSO4↓
- Фосфаты также дают белые осадки:
3Ca2+ + 2PO43- → Ca3(PO_4)2↓
7. Видео эксперименты
Рекомендуем посмотреть опыты с щелочноземельными металлами на канале Thoisoi:








