Щелочные металлы

Химия элементов IА группы: от Лития до Франция
Важно для ЕГЭ
Щелочные металлы — самые активные металлы. В соединениях они всегда проявляют постоянную степень окисления +1. Их гидроксиды являются растворимыми в воде сильными основаниями (щелочами).
1. Общая характеристика элементов IA группы
К щелочным металлам относятся элементы главной подгруппы I группы Периодической системы:
- Литий (Li)
- Натрий (Na)
- Калий (K)
- Рубидий (Rb)
- Цезий (Cs)
- Франций (Fr) — радиоактивный элемент
Строение атома
Все эти элементы имеют сходное строение внешнего электронного уровня:
На внешнем уровне находится всего один валентный s-электрон, который они легко отдают в химических реакциях, проявляя свойства сильных восстановителей.
Закономерности в группе (Li → Fr)
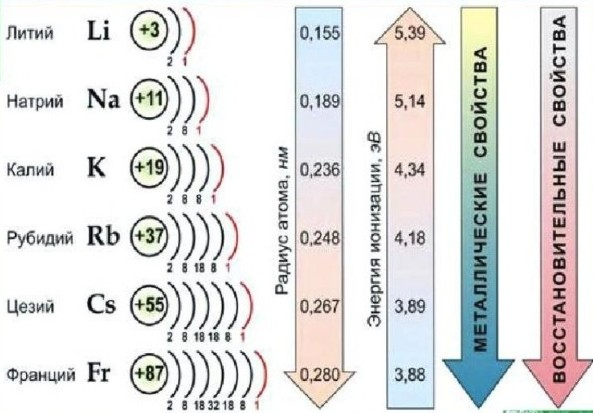
Физические свойства

Щелочные металлы — это мягкие вещества серебристо-белого цвета (на свежем срезе). Их можно резать ножом
. Обладают характерным металлическим блеском, высокой тепло- и электропроводностью. Имеют низкие температуры плавления и низкую плотность (литий, натрий и калий легче воды).Из-за высокой химической активности их хранят под слоем керосина или в запаянных ампулах (чтобы исключить контакт с кислородом и влагой воздуха).
2. Нахождение в природе
Ввиду своей исключительной активности, в свободном виде щелочные металлы в природе не встречаются. Они существуют только в виде соединений (солей).
| Название минерала | Формула / Химическое название |
|---|---|
| Каменная соль (Галит) | Формула: NaCl Химическое название: Хлорид натрия |
| Сильвин | Формула: KCl Химическое название: Хлорид калия |
| Сильвинит | Формула: NaCl · KCl Химическое название: Смешанный хлорид натрия-калия |
| Глауберова соль (Мирабилит) | Формула: Na2SO4 · 10H2O Химическое название: Декагидрат сульфата натрия |
| Селитра чилийская | Формула: NaNO3 Химическое название: Нитрат натрия |
3. Способы получения
Основной промышленный метод получения щелочных металлов — электролиз расплавов их солей (чаще всего хлоридов).
| Способ / Металл | Описание процесса и уравнения реакций |
|---|---|
| Электролиз расплава (Li, Na) |
Электролитическое получение щелочных металлов осуществляют исключительно из расплавов солей (чаще всего хлоридов), так как в водных растворах из-за активности металлов на катоде будет восстанавливаться водород:
2NaCl(расплав) → 2Na + Cl2↑
Катод (-): Na+ + e- → Na0
Анод (+): 2Cl- - 2e- → Cl20
Примечание: Аналогично получают литий из расплава LiCl.
|
| Термохимическое восстановление (K, Rb, Cs) |
Более тяжелые металлы (K, Rb, Cs) технически сложно получать электролизом. Их получают металлотермически или вакуумтермически — вытесняют из расплавов хлоридов парами более активного натрия, либо восстанавливают кальцием или цирконием:
KCl + Na t°⇄ NaCl +
K↑2CsCl + Ca t°→ CaCl2 + 2Cs↑ |
4. Химические свойства простых веществ (Металлов)
Щелочные металлы — сильнейшие восстановители. Они легко отдают единственный внешний электрон, превращаясь в положительно заряженные ионы M+.
| Реагент | Описание процесса и уравнения реакций |
|---|---|
| С галогенами |
Щелочные металлы самовоспламеняются в атмосфере галогенов уже при комнатной температуре. Образуются прочные ионные соли-галогениды:
2Na + Cl2 → 2NaCl
2K + I2 → 2KI 2Cs + F2 → 2CsF |
| С серой |
Реакция с расплавленной серой носит взрывной характер. Калий и рубидий способны реагировать с серой даже при механическом растирании:
2Na + S t°→
Na2S |
| С фосфором |
Реакция требует нагревания, после чего идет с сильным выделением теплоты. Образуются фосфиды:
3K + P t°→
K3P
 |
| С водородом |
При нагревании присоединяют водород, образуя солеобразные (ионные) гидриды. Гидриды — мощные восстановители и бурно реагируют с водой:
2Na + H2 t°→
2NaH
|
| С азотом |
Только литий способен медленно связывать азот при комнатной температуре благодаря огромной энергии решетки нитрида лития. Остальные металлы образуют нитриды только при сильном нагревании или электрическом разряде:
6Li + N2 → 2Li3N
 |
| С кислородом |
Важное различиеРеакция с кислородом специфична. Маленький ион лития образует устойчивый нормальный оксид. Более крупные образуют пероксиды или надпероксиды:
• Литий образует нормальный оксид: 4Li +
O2 → 2Li2O
• Натрий образует пероксид: 2Na + O2 → Na2O2 • Калий, Рубидий, Цезий образуют надпероксиды: K + O2 → KO2 |
| С водой |
Взаимодействие с водой идет исключительно активно. Литий реагирует спокойно, натрий плавится и бегает по поверхности, калий воспламеняет водород фиолетовым пламенем, а тяжелые металлы реагируют со взрывом:
2Na + 2H2O → 2NaOH + H2↑
|
| С кислотами |
Бурно растворяются в кислотах с выделением водорода или глубоких продуктов восстановления кислоты-окислителя. Реакция часто сопровождается взрывом выделяющейся газовой смеси:
С HCl: 2Na + 2HCl → 2NaCl + H2↑
С конц. H2SO4 (возможно образование H2S и S): 8Na + 5H2SO4(конц.) → 4Na2SO4 + H2S + 4H2O С азотной кислотой (HNO3): С концентрированной (образуется N2O): 8Na + 10HNO3(конц.) → 8NaNO3 + N2O↑ + 5H2O С разбавленной (образуется N2): 10Na + 12HNO3(разб.) → 10NaNO3 + N2↑ + 6H2O С очень разбавленной (образуется NH4NO3): 8Na + 10HNO3(оч. разб.) → 8NaNO3 + NH4NO3 + 3H2O |
Взаимодействие с органическими веществами
Щелочные металлы способны замещать водород в соединениях, обладающих даже очень слабыми кислотными свойствами:
| Реагент | Описание процесса и уравнения реакций |
|---|---|
| Со спиртами |
образование алкоголятов
2CH3OH
+ 2Na → 2CH3ONa + H2↑
|
| С фенолом |
образование фенолятов
2C6H5OH + 2Na → 2C6H5ONa +
H2↑
 |
| С алкинами |
с концевой тройной связью
HC≡CH + 2Na →
NaC≡CNa + H2↑
|
| С галогеналканами |
реакция Вюрца
2CH3Cl +
2Na → C2H6 + 2NaCl
|
Щелочные металлы способны замещать водород в соединениях, обладающих даже очень слабыми кислотными свойствами:
- Со спиртами (образование алкоголятов):
2CH3OH + 2Na → 2CH3ONa + H2↑ - С фенолом (образование фенолятов):
2C6H5OH + 2Na → 2C6H5ONa + H2↑ - С алкинами (с концевой тройной связью):
HC≡CH + 2Na → NaC≡CNa + H2↑ - С галогеналканами (реакция Вюрца):
2CH3Cl + 2Na → C2H6 + 2NaCl
5.1. Оксиды щелочных металлов (M2O)
Оксиды (например, Na2O, K2O) — это твердые вещества, проявляющие ярко выраженные основные свойства.
Получение: Прямым окислением можно получить только Li2O. Оксиды других металлов получают косвенно:
| Способ / Условие | Описание процесса и уравнения реакций |
|---|---|
| Прямое окисление |
Прямым окислением кислородом можно получить только оксид лития. Оксиды других
металлов получают косвенно.
|
| Нагревание пероксида с металлом |
Оксид натрия получают косвенным путем: сплавлением пероксида натрия с металлическим натрием в отсутствие кислорода (иначе натрий сгорит до пероксида):
Na2O2 + 2Na → 2Na2O
|
| Нагревание нитрата с металлом |
Нитраты щелочных металлов являются сильными окислителями при нагревании. Металлический натрий восстанавливает азот из нитрата до молекулярного азота, сам окисляясь до оксида:
2NaNO3 + 10Na → 6Na2O +
N2↑
|
| Взаимодействие металла с расплавом щелочи |
Расплавы щелочей также могут быть восстановлены избытком чистого щелочного металла с образованием оксида и выделением газообразного водорода:
2Na + 2NaOH → 2Na2O + H2↑
|
| Разложение гидроксида |
Из-за малого радиуса иона лития его гидроксид наименее термически устойчив среди щелочных. Он разлагается при прокаливании до оксида и воды. Остальные щелочи плавятся и кипят без разложения:
2LiOH t°→
Li2O + H2O
|
Химические свойства:
| Свойство / Реагент | Описание процесса и уравнения реакций |
|---|---|
| С водой |
Оксиды щелочных металлов являются типичными сильноосновными оксидами. Они экзотермично взаимодействуют с водой, образуя растворимые щелочи:
Na2O + H2O → 2NaOH
 |
| С кислотными оксидами |
Легко вступают во взаимодействие с кислотными оксидами с образованием средних солей:
Na2O + CO2 →
Na2CO3
|
| С амфотерными оксидами и гидроксидами (при сплавлении) |
При сплавлении (твердофазная реакция) основные оксиды реагируют с амфотерными. При этом образуются безводные соли — алюминаты, цинкаты и т.д.:
Na2O + Al2O3 t°→ 2NaAlO2 (метаалюминат натрия)K2O + Zn(OH)2 t°→ K2ZnO2 + H2O (цинкат калия)  |
| С кислотами |
Типичная реакция нейтрализации основного оксида кислотой, приводящая к образованию соли и воды:
K2O + 2HCl → 2KCl + H2O
|
| Окисление кислородом |
Оксиды натрия, калия и более тяжелых щелочных металлов способны присоединять кислород при нагревании, переходя в более богатые кислородом пероксиды и надпероксиды. Оксид лития не переходит в пероксид прямым окислением:
2Na2O + O2 →
2Na2O2
|
5.2. Пероксиды щелочных металлов (M2O2)
Содержат кислород в степени окисления -1 (группа -O-O-). Пероксид натрия Na2O2 — желтоватый порошок.
Свойства:
| Свойство / Реагент | Описание процесса и уравнения реакций |
|---|---|
| Реакция с водой (гидролиз) |
На холоде: Na2O2 + 2H2O → 2NaOH + H2O2 При нагревании (диспропорционирование): 2Na2O2 + 2H2O → 4NaOH + O2↑  |
| С углекислым газом |
Регенерация воздуха на подводных лодках:
2Na2O2 + 2CO2 →
2Na2CO3 + O2↑
|
| С минеральными кислотами |
На холоде (обменная реакция): Na2O2 + 2HCl → 2NaCl + H2O2 При нагревании (диспропорционирование): 2Na2O2 + 2H2SO4(разб.гор.) → 2Na2SO4 + 2H2O + O2↑ |
| Термическое разложение | 2Na2O2 t°→ 2Na2O + O2↑ |
| Окислительные свойства (с восстановителями) |
С угарным газом: Na2O2 + CO →
Na2CO3 С сернистым газом: Na2O2 + SO2 → Na2SO4 С серой: 2Na2O2 + S → Na2SO3 + Na2O С иодидами в кислой среде: Na2O2 + 2H2SO4 + 2NaI → I2 + 2Na2SO4 + 2H2O  Na2O2 + 2H2SO4 + 2FeSO4 → Fe2(SO4)3 + Na2SO4 + 2H2O С солями хрома (III) в щелочной среде: 3Na2O2 + 2Na3[Cr(OH)6] → 2Na2CrO4 + 8NaOH + 2H2O |
| Восстановительные свойства |
С сильными окислителями (например, с перманганатом калия в кислой среде выделяется
кислород):
5Na2O2 + 2KMnO4 +
8H2SO4 → 5O2↑ + 2MnSO4 +
5Na2SO4 + K2SO4 + 8H2O
 |
5.3. Гидроксиды (Щелочи)
Гидроксиды щелочных металлов (LiOH, NaOH, KOH, RbOH, CsOH) — твердые белые вещества, гигроскопичные, прекрасно растворимые в воде. Являются сильными основаниями (щелочами).
Тривиальные названия: NaOH — едкий натр (каустическая сода), KOH — едкое кали.
Способы получения:
| Способ / Метод | Описание процесса и уравнения реакций |
|---|---|
| Электролиз растворов хлоридов |
Основной промышленный способ:
2NaCl + 2H2O эл.→ 2NaOH
+ H2↑ + Cl2↑
|
| Гидратация (взаимодействие с водой) |
Металлы: 2Na + 2H2O → 2NaOH +
H2↑ Оксиды: Na2O + H2O → 2NaOH Пероксиды: Na2O2 + H2O → 2NaOH + H2O2 Гидриды: 2NaH + 2H2O → 2NaOH + H2↑ |
| Обменные реакции (каустификация) |
Взаимодействие растворимых солей щелочных металлов с гидроксидами кальция (известковым молоком) или бария. Реакция идет до конца за счет выпадения нерастворимого карбоната/сульфата кальция или бария, оставляя в растворе щелочь:
K2CO3 + Ca(OH)2 →
CaCO3↓ + 2KOH
|
Химические свойства:
| Реагент / Условие | Описание процесса и уравнения реакций |
|---|---|
| Диссоциация |
Сильные электролиты, диссоциируют нацело.
NaOH ⇄ Na+ + OH-
Среда щелочная, изменяют окраску индикаторов (лакмус — синий,
фенолфталеин — малиновый, метилоранж — желтый).
|
| С кислотами (любыми) |
Реакция нейтрализации: щелочи бурно, с выделением тепла, реагируют и с сильными, и со слабыми кислотами. В зависимости от соотношения щелочи (избыток/недостаток) и основности кислоты образуются средние или кислые соли:
3KOH + H3PO4 → K3PO4
+ 3H2O (избыток щелочи)2KOH + H3PO4 → K2HPO4 + 2H2O KOH + H3PO4 → KH2PO4 + H2O (избыток кислоты) |
| С кислотными оксидами |
Растворимые щелочи легко поглощают кислотные оксиды (CO₂, SO₂, NO₂). Избыток щелочи дает среднюю соль (карбонат), а избыток газа — кислую (гидрокарбонат). Оксид NO₂ диспропорционирует во влажной среде, давая смесь нитрита и нитрата:
2NaOH(изб.) + CO2 →
Na2CO3 + H2ONaOH + CO2(изб.) → NaHCO3 С оксидом NO2 (диспропорционирование): 2NO2 + 2NaOH → NaNO3 + NaNO2 + H2O В присутствии O2: 4NO2 + 4KOH + O2 → 4KNO3 + 2H2O |
| С амфотерными оксидами и гидроксидами |
Щелочи реагируют с амфотерными соединениями с проявлением кислотных свойств последних. Условия реакции определяют состав соли: в растворах за счет избытка воды и координационного числа образуются гидроксокомплексы, а при сплавлении (без воды) — безводные алюминаты, цинкаты и др.:
В расплаве:2NaOH + Al2O3 t°→ 2NaAlO2 + H2O В растворе (образуются комплексные соли): 2NaOH + Al2O3 + 3H2O → 2Na[Al(OH)4] NaOH + Al(OH)3 → Na[Al(OH)4] |
| С амфотерными металлами (Zn, Al, Be) |
Важное свойство щелочей: они способны растворять металлы, оксиды которых амфотерны. Водород выделяется за счет того, что щелочь способствует окислению металла водой с последующим переходом гидроксида металла в комплекс в растворе (или алюминат в расплаве):
В расплаве:2KOH + Zn t°→ K2ZnO2 + H2↑ В растворе: 2NaOH + 2Al + 6H2O → 2Na[Al(OH)4] + 3H2↑ |
| С кислыми солями |
Щелочь нейтрализует ("донейтрализует") кислые соли, содержащие протоны, превращая их в средние соли с образованием воды:
KOH + KHCO3 → K2CO3 +
H2O
|
| С растворимыми солями |
Реакционные среды обмениваются ионами (реакция обмена). Она протекает до конца, только если продукт реакции уходит из среды — выпадает в осадок (нерастворимые гидроксиды переходных металлов) или выделяется газ (аммиак при нагревании солей аммония со щелочами):
CuCl2 + 2NaOH → Cu(OH)2↓ + 2NaCl
(осадок)  |
| С неметаллами |
Щелочи активно взаимодействуют с неметаллами: кремний растворяется с выделением водорода (щелочь снимает гидроксидную пленку). Фтор является более сильным окислителем, окисляя кислород щелочи до фторида кислорода (II). Фосфор, сера и галогены (от Cl до I) диспропорционируют (самоокисляются-самовосстанавливаются) в растворах щелочей, давая соли разных степеней окисления:
Si (окисляется):Si + 2NaOH + H2O → Na2SiO3 + 2H2↑  2F2 + 2NaOH → 2NaF + OF2↑ + H2O (также возможно выделение O2) P, S, Cl2, Br2, I2 (диспропорционируют): 4P + 3KOH + 3H2O → 3KH2PO2 + PH3↑ 3S + 6NaOH t°→ 2Na2S + Na2SO3 + 3H2O  3Cl2 + 6KOH(гор.) → 5KCl + KClO3 + 3H2O |
| Термическая устойчивость |
Плавится без разложения (NaOH, KOH).
Исключение: LiOH разлагается:2LiOH 600°C→ Li2O + H2O |
| Электролиз расплава | 4NaOH эл.→ 4Na + O2↑ + 2H2O |
5.4. Соли щелочных металлов
Почти все соли щелочных металлов растворимы в воде. Особый интерес представляет термическое разложение нитратов.
Разложение нитратов при нагревании
1. Нитрат лития (как и нитраты магния, меди) разлагается до оксида:
4LiNO3 → 2Li2O + 4NO2 + O2
2. Нитраты остальных щелочных металлов (Na, K, Rb, Cs) разлагаются до нитритов:
2NaNO3 → 2NaNO2 + O2
2KNO3 → 2KNO2 + O2
6. Качественные реакции (Окрашивание пламени)
Ионы щелочных металлов окрашивают пламя горелки в характерные цвета, что используется для их качественного обнаружения.

7. Видео эксперименты
Рекомендуем посмотреть опыты с щелочными металлами на канале Thoisoi:
















