1. Типы реакций по количеству и составу участников
В зависимости от того, как меняется состав веществ в ходе превращения, выделяют две большие группы: процессы без изменения химического состава и процессы с изменением состава участников.
1.1. Превращения без изменения состава (A → B)
В неорганике к этой категории принадлежат аллотропные превращения — переход простого вещества из одной кристаллической формы в другую:
В органике аналогом служат изомеризационные превращения. При воздействии катализатора или внешних условий молекула перестраивается в другой структурный изомер без изменения брутто-формулы.
превращение н-бутана в изобутан
Реакции соединения (A + B + ... → D)
При таких превращениях несколько исходных веществ объединяются в одно сложное соединение.
- В неорганике: окисление простых веществ кислородом (горение), взаимодействие кислотных и основных оксидов и т.п.
- В органике подобные процессы именуют реакциями присоединения: насыщение водородом (гидрирование), присоединение воды (гидратация), галогеноводородов, а также полимеризация.
Реакции разложения (A → B + C + ...)
Здесь одно сложное вещество распадается на несколько более простых компонентов.
В органике различают:
- Деструкция (крекинг) — разрыв углеродного скелета с образованием меньших молекул.
- Элиминирование (отщепление) — удаление атомов или групп без разрушения основной цепи (дегидрирование, дегидратация и др.).
Реакции замещения (AB + C → AC + B)
В таких процессах атом или функциональная группа одного соединения вытесняется атомом или группой другого вещества.
В неорганике: более активный элемент вытесняет менее активный из его соединений.
В органике: один фрагмент молекулы замещается другой частицей.
Реакции обмена (AB + CD → AC + BD)
Два сложных соединения обмениваются составными частями, образуя новые продукты.
Сюда входят ионные взаимодействия в растворах, нейтрализация кислот основаниями и другие аналогичные процессы.
2. Типы реакций по изменению степеней окисления
Исходя из того, меняются ли степени окисления атомов, все превращения делят на две группы:
2.1. Окислительно-восстановительные реакции (ОВР)
Определение
Окислительно-восстановительные реакции — это реакции, протекающие с изменением степеней окисления атомов элементов, входящих в состав реагирующих веществ.
Важно!
Обратите внимание! К ОВР обычно относят процессы соединения, разложения, замещения, а также любые превращения с участием простых веществ.
Органические реакции восстановления: процессы, при которых увеличивается число атомов водорода или уменьшается число атомов кислорода.
2.2. Реакции без изменения степеней окисления
К ним принадлежат кислотно-основные (протолитические) взаимодействия и реакции обмена.
3. Типы реакций по энергетическому эффекту
В зависимости от того, выделяется или поглощается теплота, выделяют экзотермические и эндотермические превращения.
3.1. Экзотермические процессы (+Q)
Сопровождаются высвобождением тепловой энергии в окружающую среду. Характерные примеры: большинство реакций соединения, горение, нейтрализация, взаимодействие щелочных металлов с водой, алюминотермия.
Исключения (эндотермические соединения):
3.2. Эндотермические процессы (–Q)
Протекают с поглощением тепловой энергии из окружающей среды. Характерные примеры: большинство разложений, гидролиз, электролиз, фотолиз, термический крекинг.
4. Типы реакций по агрегатному состоянию участников
Вещества способны пребывать в трёх агрегатных состояниях: твёрдом, жидком и газообразном. По этому признаку химические превращения подразделяют на:
4.1. Гомогенные процессы
Все участники и продукты находятся в одной фазе, поэтому взаимодействие частиц происходит во всём объёме системы. К гомогенным относят взаимодействия типа жидкость + жидкость и газ + газ.
4.2. Гетерогенные процессы
Участники и продукты находятся в разных фазах, а взаимодействие частиц происходит только на границе раздела этих фаз. К гетерогенным относят взаимодействия типа: газ + жидкость, газ + твёрдое, твёрдое + твёрдое, твёрдое + жидкость.
5. Типы реакций по участию катализатора
Катализатор — вещество, которое увеличивает скорость превращения, но не расходуется и не входит в конечные продукты. Он временно связывается с реагентами, а затем высвобождается.
Важно!
Упрощённая схема действия катализатора К:
A + K → AK
AK + B → AB + K
5.1. Каталитические процессы
Превращения, протекающие при участии катализатора.
5.2. Некаталитические процессы
Превращения, протекающие без добавления катализатора.
5.3. Ферментативные процессы
Биохимические превращения в живых клетках идут при участии особых белковых катализаторов — ферментов. Такие превращения называют ферментативными.
6. Типы реакций по направлению протекания
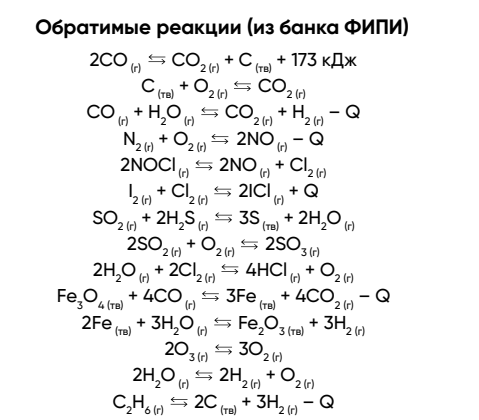
6.1. Обратимые процессы
Могут идти как в прямом, так и в обратном направлении: образовавшиеся продукты способны вновь превращаться в исходные вещества при тех же условиях. Типичные обратимые превращения: большинство гомогенных газовых реакций, этерификация, гидролиз, гидратация ⇌ дегидратация.
6.2. Необратимые процессы
Протекают преимущественно в одном направлении: продукты практически не способны вернуться к исходным веществам при данных условиях.
Важно!
Признаки необратимости: горение, взрывы, выпадение осадка ↓, выделение газа ↑, образование воды.
Итоговая таблица классификации
| Критерий классификации | Виды реакций |
|---|---|
| По количеству и составу участников | Соединения, разложения, замещения, обмена, изомеризации |
| По изменению степеней окисления | ОВР (с переносом электронов), не ОВР (без переноса) |
| По энергетическому эффекту | Экзотермические (+Q), эндотермические (–Q) |
| По агрегатному состоянию | Гомогенные (одна фаза), гетерогенные (разные фазы) |
| По участию катализатора | Каталитические, некаталитические, ферментативные |
| По направлению протекания | Обратимые (⇌), необратимые (→) |
Специфические названия реакций
В химии многие превращения имеют собственные названия, отражающие суть процесса. Ниже приведён справочник наиболее важных терминов.
Реакции присоединения
| Название | Описание | Пример |
|---|---|---|
| Гидрирование | Присоединение водорода (H2) по кратной связи | CH2=CH2 + H2 → C2H6 |
| Гидратация | Присоединение воды (H2O) | CH2=CH2 + H2O → C2H5OH |
| Галогенирование | Присоединение галогена (Cl2, Br2) | CH2=CH2 + Br2 → CH2Br–CH2Br |
| Гидрогалогенирование | Присоединение галогеноводорода (HCl, HBr) | CH2=CH2 + HBr → CH3–CH2Br |
| Полимеризация | Соединение множества молекул мономера в полимер | nCH2=CH2 → (–CH2–CH2–)n |
Реакции отщепления (элиминирования)
| Название | Описание | Пример |
|---|---|---|
| Дегидрирование | Отщепление водорода (H2) | C2H6 → CH2=CH2 + H2 |
| Дегидратация | Отщепление воды (H2O) | C2H5OH → CH2=CH2 + H2O |
| Дегалогенирование | Отщепление галогена (обычно с Zn) | CH2Br–CH2Br + Zn → CH2=CH2 + ZnBr2 |
| Дегидрогалогенирование | Отщепление галогеноводорода (HCl, HBr) | CH3–CH2Cl + KOH(спирт) → CH2=CH2 + KCl + H2O |
| Крекинг | Разрыв углеродной цепи при нагревании | C10H22 → C5H10 + C5H12 |
| Декарбоксилирование | Отщепление CO2 от карбоновой кислоты | CH3COONa + NaOH → CH4 + Na2CO3 |
Реакции замещения
| Название | Описание | Пример |
|---|---|---|
| Галогенирование (замещение) | Замена атома H на галоген | CH4 + Cl2 → CH3Cl + HCl |
| Нитрование | Замещение H на нитрогруппу (–NO2) | C6H6 + HNO3 → C6H5NO2 + H2O |
| Сульфирование | Замещение H на сульфогруппу (–SO3H) | C6H6 + H2SO4 → C6H5SO3H + H2O |
| Алкилирование | Введение алкильной группы в молекулу | C6H6 + CH3Cl → C6H5CH3 + HCl |
| Радикальное замещение (SR) | Замещение по радикальному механизму (цепная реакция) | Хлорирование алканов на свету |
| Электрофильное замещение (SE) | Замещение с атакой электрофила | Реакции бензола с электрофилами |
| Нуклеофильное замещение (SN) | Замещение с атакой нуклеофила | CH3Br + NaOH → CH3OH + NaBr |
Реакции обмена и ионные
| Название | Описание | Пример |
|---|---|---|
| Нейтрализация | Взаимодействие кислоты с основанием | HCl + NaOH → NaCl + H2O |
| Ионного обмена | Обмен ионами между электролитами в растворе | BaCl2 + Na2SO4 → BaSO4↓ + 2NaCl |
| Гидролиз | Разложение вещества водой | Na2CO3 + H2O ⇌ NaHCO3 + NaOH |
| Этерификация | Образование сложного эфира из кислоты и спирта | CH3COOH + C2H5OH ⇌ CH3COOC2H5 + H2O |
| Омыление | Гидролиз сложного эфира в щелочной среде | CH3COOC2H5 + NaOH → CH3COONa + C2H5OH |
Окислительно-восстановительные реакции
| Название | Описание | Пример |
|---|---|---|
| Горение | Окисление кислородом с выделением тепла и света | CH4 + 2O2 → CO2 + 2H2O |
| Окисление | Потеря электронов, увеличение СО | Fe0 → Fe3+ + 3e− |
| Восстановление | Приобретение электронов, уменьшение СО | Cu2+ + 2e− → Cu0 |
| Диспропорционирование | Один элемент одновременно окисляется и восстанавливается | Cl2 + 2NaOH → NaCl + NaClO + H2O |
| Сопропорционирование | Два атома одного элемента с разными СО дают одинаковую СО | 2H2S + SO2 → 3S + 2H2O |
Другие типы реакций
| Название | Описание | Пример |
|---|---|---|
| Изомеризация | Перестройка структуры без изменения формулы | н-бутан → изобутан |
| Поликонденсация | Образование полимера с выделением побочного продукта | Синтез полиэфиров, полиамидов |
| Риформинг | Превращение алканов в арены и изоалканы | н-гексан → бензол + H2 |
| Пиролиз | Разложение органических веществ при высокой температуре без кислорода | CH4 → C + 2H2 |
| Электролиз | ОВР под действием электрического тока | 2NaCl → 2Na + Cl2 |
| Фотолиз | Разложение под действием света | 2AgBr → 2Ag + Br2 |