Скорость химических реакций (Химическая кинетика)
1. Что такое скорость реакции?
Скорость химической реакции ($\upsilon$) показывает, как быстро протекает процесс, то есть как быстро расходуются исходные вещества или образуются продукты реакции.
Важно!
Реакция происходит при столкновении частиц. Но не каждое столкновение приводит к реакции, а только эффективное (когда частицы обладают достаточной энергией).
Гомогенные реакции (однородная среда)
Если реагенты находятся в одной фазе (газ + газ или жидкость + жидкость), скорость определяется как изменение концентрации вещества ($\Delta C$) за единицу времени ($\Delta t$):
Гетерогенные реакции (разные фазы)
Если реакция идет на границе раздела фаз (например, твердое + газ), скорость зависит от изменения количества вещества ($\Delta \nu$) на единицу площади поверхности ($S$) за единицу времени:
Факторы, влияющие на скорость реакции
Скорость реакции зависит от условий, в которых она протекает. Рассмотрим основные факторы.
1. Температура
При повышении температуры частицы движутся быстрее и сталкиваются чаще. Но главное — резко возрастает доля активных частиц, способных преодолеть энергетический барьер.
Правило Вант-Гоффа
При повышении температуры на каждые 10°C скорость реакции возрастает в 2–4 раза.
Важно!
Это правило работает и для экзотермических, и для эндотермических реакций. При нагревании скорость всегда растет.
2. Концентрация реагентов
Чем выше концентрация реагирующих веществ (для газов и растворов), тем больше частиц в единице объема и тем чаще они сталкиваются.
Закон действующих масс
Скорость реакции прямо пропорциональна произведению концентраций реагирующих веществ в степенях их коэффициентов.
Для реакции $aA + bB \to D$:
Концентрации твердых веществ в уравнение скорости гетерогенной реакции не входят, так как они реагируют только на поверхности и их концентрация постоянна.
Однако, если твердое вещество то по мере его растворения концентрация вещества в растворе увеличивается, что может влиять на скорость реакций, протекающих уже в жидкой фазе.
3. Давление (только для газов)
Влияет только на реакции с участием газов. Изменение давления равносильно изменению концентрации газа.
- Повышение давления (сжатие = уменьшение объема сосуда) $\to$ увеличение концентрации газов $\to$ ускорение реакции.
- Понижение давления (расширение = увеличение объема сосуда) $\to$ уменьшение концентрации газов $\to$ замедление реакции.
Изменение объема сосуда обратно давлению:
Уменьшение объема сосуда в N раз = Увеличение давления в N раз = Увеличение скорости (для
газов).
Увеличение объема сосуда в N раз = Уменьшение давления в N раз = Уменьшение скорости (для газов).
Давление влияет (все газы)
Давление влияет (есть газ)
Давление НЕ влияет (нет газов)
4. Катализаторы
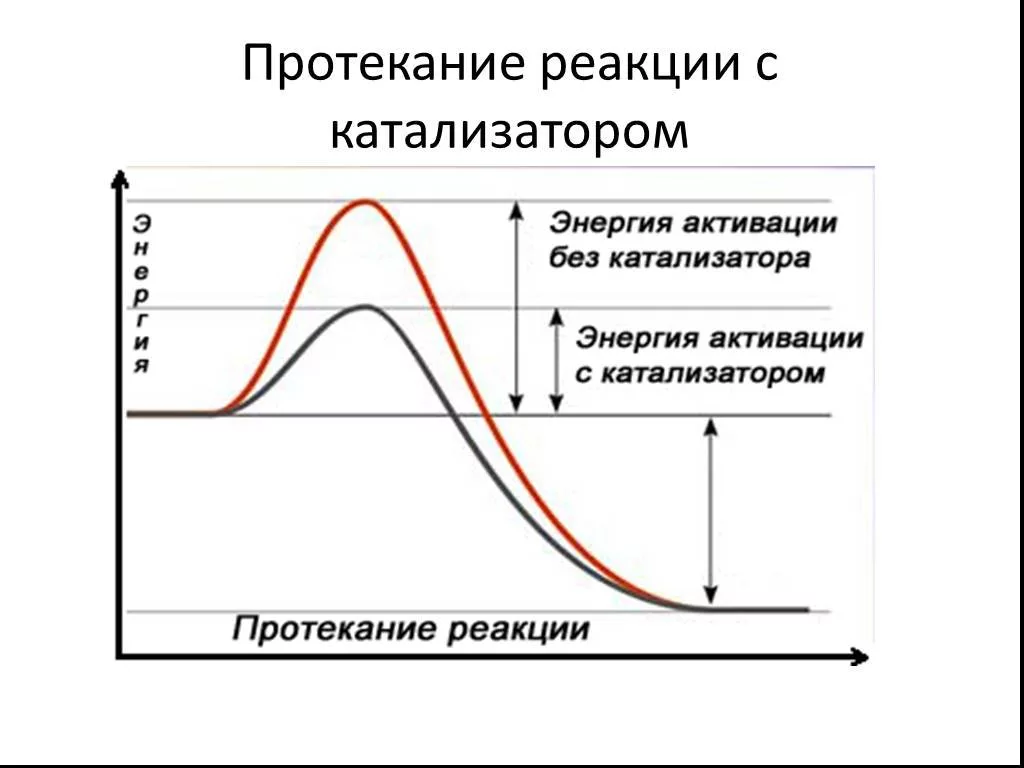
Катализаторы — вещества, ускоряющие реакцию, но не расходующиеся в ней. Они направляют процесс по другому механизму с меньшей энергией активации.
- Гомогенный катализ: реагенты и катализатор в одной фазе (газ+газ или раствор+раствор).
- Гетерогенный катализ: катализатор твердый, реагенты — газы или жидкости (реакция идет на поверхности).
Ингибиторы - вещества, замедляющие реакцию (но они НЕ называются «отрицательными катализаторами»).
5. Площадь соприкосновения (для гетерогенных)
Актуально для реакций с участием твердых веществ. Чем сильнее измельчено твердое вещество, тем больше площадь контакта и выше скорость.
- Растворение порошка цинка в кислоте идет быстрее, чем растворение гранул.
- Сжигание угольной пыли происходит мгновенно (взрыв), в отличие от горения куска угля.
- Для жидких реагентов (несмешивающихся) помогает перемешивание.
6. Природа реагирующих веществ
Скорость зависит от химической активности веществ и прочности разрываемых связей (энергии активации).
- Реакции ионного обмена (в растворах электролитов) идут мгновенно (связи не рвутся, ионы просто соединяются).
- Чем активнее металл/неметалл, тем быстрее реакция (например, Na реагирует с водой быстрее, чем Mg).