Электролитическая диссоциация
1. Что такое электролиты и неэлектролиты?
В начале XIX века Майкл Фарадей установил, что растворы некоторых веществ способны проводить электрический ток. Позже Сванте Аррениус создал теорию электролитической диссоциации.
Электролиты
Вещества, растворы или расплавы которых проводят электрический ток.
К ним относятся вещества с ионной или ковалентной сильнополярной связью.
Неэлектролиты
Вещества, растворы и расплавы которых не проводят электрический ток.
Имеют ковалентную неполярную или слабополярную связь.
Пример: Раствор сахара в воде ток не проводит.
Ионы — это заряженные частицы:
- Катионы (+) — положительно заряженные ионы (движутся к катоду). Пример: $Na^+$, $H^+$, $Ca^{2+}$.
- Анионы (–) — отрицательно заряженные ионы (движутся к аноду). Пример: $Cl^-$, $SO_4^{2-}$, $OH^-$.
2. Механизм диссоциации в растворах
Для веществ с ионной связью (NaCl):
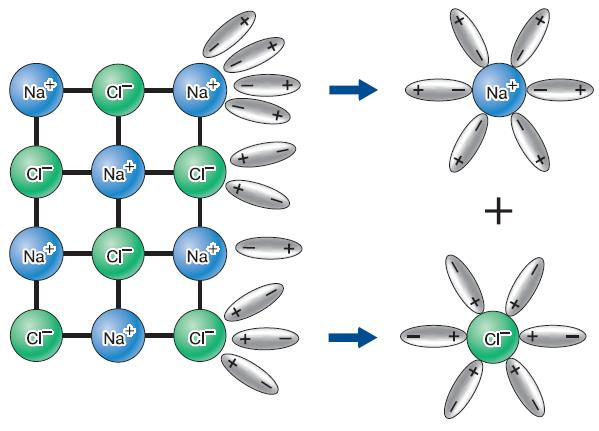
- Ориентация: Молекулы воды окружают кристалл соли. Отрицательные концы воды (кислород) притягиваются к катионам ($Na^+$), положительные (водород) — к анионам ($Cl^-$).
- Гидратация: Образуются связи между ионами и водой.
- Распад: Связь между ионами в кристалле ослабевает, и они переходят в раствор в виде гидратированных ионов.
В расплавах процесс проще: тепловая энергия разрушает кристаллическую решетку, и ионы становятся подвижными без участия воды.
3. Сильные и слабые электролиты
Не все электролиты распадаются на ионы одинаково хорошо. Мерой распада является степень диссоциации ($\alpha$).
Где $n$ — число распавшихся молекул, $N$ — общее число растворенных молекул.
Кислоты
Основания
Соли и Другое
4. Уравнения электролитической диссоциации
Диссоциируют на катионы водорода ($H^+$) и анионы кислотных остатков.
$HNO_3 \rightarrow H^+ + NO_3^-$
Многоосновные кислоты диссоциируют ступенчато (постепенно отщепляя $H^+$). Процесс обратим, первая ступень идет легче всего.
- I ступень: $H_3PO_4 \leftrightarrows H^+ + H_2PO_4^-$ (дигидрофосфат-ион)
- II ступень: $H_2PO_4^- \leftrightarrows H^+ + HPO_4^{2-}$ (гидрофосфат-ион)
- III ступень: $HPO_4^{2-} \leftrightarrows H^+ + PO_4^{3-}$ (фосфат-ион)
Диссоциируют на катионы металла (или $NH_4^+$) и гидроксид-анионы ($OH^-$).
$Ba(OH)_2 \rightarrow Ba^{2+} + 2OH^-$
Многокислотные слабые основания также диссоциируют ступенчато:
- I ступень: $Fe(OH)_2 \leftrightarrows Fe(OH)^+ + OH^-$ (гидроксо-катион железа)
- II ступень: $Fe(OH)^+ \leftrightarrows Fe^{2+} + OH^-$
Диссоциируют на катионы металла (или $NH_4^+$) и анионы кислотного остатка.
Средние соли (диссоциируют полностью в одну стадию):
$Al_2(SO_4)_3 \rightarrow 2Al^{3+} + 3SO_4^{2-}$
Кислые соли (содержат H) — диссоциируют ступенчато:
- I ступень (как соль, полностью): $NaHCO_3 \rightarrow Na^+ + HCO_3^-$
- II ступень (как слабая кислота, обратимо): $HCO_3^- \leftrightarrows H^+ + CO_3^{2-}$
Комплексные соли (диссоциация внешней сферы):
Внутренняя сфера $[Al(OH)_4]^-$ очень прочная и диссоциирует крайне слабо (вторичная диссоциация).