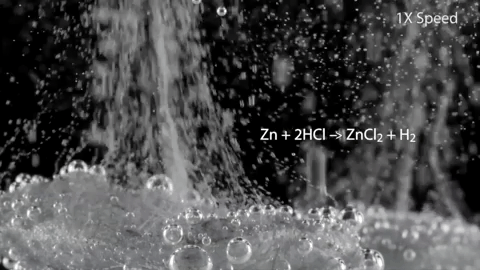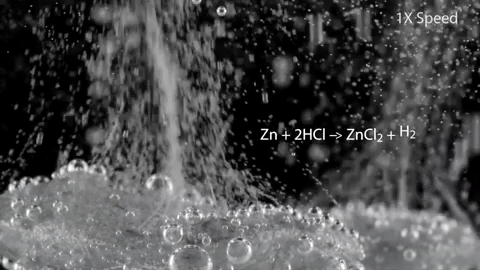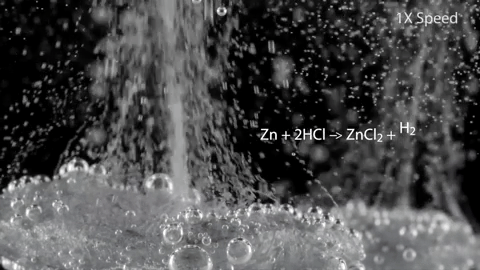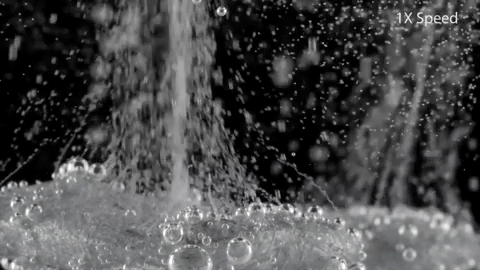Цинк, кадмий и ртуть
Элементы IIB-группы (побочная подгруппа II группы): амфотерный цинк, токсичный кадмий и жидкая ртуть
Важно для ЕГЭ
Цинк — амфотерный металл. Его оксид ZnO и гидроксид
Zn(OH)2 реагируют как с кислотами, так и щелочами (в том числе в расплаве и в растворе с
образованием комплексов).
Для металлов подгруппы цинка наиболее характерна степень окисления +2.
Ртуть — металл, находящийся при нормальных условиях в жидком состоянии. Для ртути характерны степени
окисления +1 и +2. Ртуть не вытесняет водород из кислот.
1. Строение атомов и положение в ПС
Цинк (Zn), кадмий (Cd) и ртуть (Hg) расположены в IIB-группе периодической системы. У этих элементов полностью заполняется предвнешний d-подуровень (d10), а на внешнем энергетическом уровне находятся два s-электрона (ns2).
Электронные конфигурации
+30Zn: 1s22s22p63s23p63d104s2
+80Hg: [Xe]4f145d106s2
Особенность
2. Физические свойства
| Свойство | Цинк (Zn) | Кадмий (Cd) | Ртуть (Hg) |
|---|---|---|---|
| Агрегатное состояние | Твёрдое металл | Твёрдый металл | Жидкое (единственный жидкий металл) |
| Цвет | Серебристо-белый с синеватым отливом | Серебристо-белый, мягкий | Серебристо-белый |
| t° плавления | 419°C | 321°C | –38,8°C |
| Плотность (г/см³) | 7,14 (тяжёлый) | 8,65 (тяжёлый) | 13,53 (очень тяжёлая) |


| Металл | Содержание и состояние в природе | Основные минералы (руды) |
|---|---|---|
| Цинк (Zn) |
Встречается преимущественно в виде сульфидных руд. Из-за высокой химической активности в самородном виде не встречается.
|
|
| Кадмий (Cd) |
Редкий элемент. Не имеет собственных месторождений, является постоянным спутником цинка в его рудах (изоморфно замещает цинк в сфалерите).
|
|
| Ртуть (Hg) |
Относительно редкий элемент, редко встречается в самородном состоянии (в виде мелких капель). С большинством металлов образует сплавы — амальгамы (кроме железа).
|
|
4. Химические свойства простых веществ (Zn, Cd, Hg)
Цинк и кадмий — металлы средней активности (стоят до водорода в ряду напряжений), ртуть — малоактивный (благородный) металл (стоит после водорода).
| Свойство | Уравнения реакций и особенности |
|---|---|
| С неметаллами |
Цинк активно реагирует при нагревании, ртуть реагирует с кислородом только около 300°C, а с серой — даже без нагревания (демеркуризация):
2Zn + O2 t°→ 2ZnO (горение пыли)Zn + I2 H₂O→ ZnI2 (катализируется водой) 2Hg + O2 ~300°C→ 2HgO (красный оксид)  Hg + S → HgS (при комн. температуре)  |
| С водой |
Только цинк реагирует с парами воды при температуре красного каления:
Zn + H2O(пар) t°→ ZnO + H2↑
|
| С кислотами-неокислителями |
Цинк (и кадмий) вытесняет водород. Ртуть с ними не реагирует:
Zn + 2HCl → ZnCl2 + H2↑Zn + H2SO4(разб.) → ZnSO4 + H2↑  |
| Со щелочами (амфотерность) |
Цинк растворяется в щелочах, выделяя водород (отличие от Cd и Hg). В растворе — комплекс, в расплаве — цинкат:
Zn + 2NaOH + 2H2O → Na2[Zn(OH)4] + H2↑Zn + 2NaOH сплавл.→ Na2ZnO2 + H2↑ |
| С кислотами-окислителями |
Реагируют все три металла. Цинк может восстанавливать азотную кислоту до различных продуктов (вплоть до N₂O или аммиака):
4Zn + 10HNO3(разб.) → 4Zn(NO3)2 + NH4NO3 + 3H2OHg + 2H2SO4(конц.) t°→ HgSO4 + SO2↑ + 2H2O  |
| Окислительно-восстановительные В растворах |
Цинк вытесняет менее активные металлы из солей, а в щелочной среде восстанавливает нитраты до аммиака:
Zn + CuSO4 → ZnSO4 + Cu↓ 4Zn + KNO3 + 7KOH + 6H2O → 4K2[Zn(OH)4] + NH3↑ |
5. Оксид и гидроксид цинка (амфотерные)
Оба соединения обладают ярко выраженными амфотерными свойствами.
Оксид цинка (ZnO)
Белый тугоплавкий порошок, нерастворимый в воде. Амфотерный оксид.
| Свойство | Уравнения реакций |
|---|---|
| Получение |
Термическое разложение гидроксида или нитратов:
Zn(OH)2 t°→ ZnO + H2O2Zn(NO3)2 t°→ 2ZnO + 4NO2↑ + O2↑  |
| С кислотами и кисл. оксидами основные свойства |
Легко реагирует, образуя соли цинка:
ZnO + 2HCl → ZnCl2 + H2O ZnO + SO3 → ZnSO4 |
| Со щелочами и осн. оксидами кислотные свойства |
В расплаве с карбонатами, оксидами или твердыми щелочами образует цинкаты, в водном растворе щелочей — тетрагидроксоцинкаты:
ZnO + Na2O t°→ Na2ZnO2ZnO + 2NaOH(тв) t°→ Na2ZnO2 + H2O ZnO + 2NaOH + H2O → Na2[Zn(OH)4] |
| Восстановление |
Углеродом или угарным газом при нагревании:
ZnO + C t°→ Zn + COZnO + CO t°→ Zn + CO2 |
Гидроксид цинка (Zn(OH)2)
Белый студенистый осадок. Растворяется как в кислотах, так и в щелочах.
| Свойство | Уравнения реакций |
|---|---|
| Амфотерность |
Растворяется в растворах кислот и щелочей:
Zn(OH)2 + 2HCl → ZnCl2 + 2H2OZn(OH)2 + 2NaOH → Na2[Zn(OH)4]  |
| Избыток аммиака |
Растворяется в водном растворе аммиака, образуя прочный аммиачный комплекс (отличие от алюминия!):
Zn(OH)2 + 4NH3 → [Zn(NH3)4](OH)2 |
| Разрушение комплексов получение гидроксида |
При действии на тетрагидроксоцинкаты слабых кислот (или избытка CO₂, или недостатка сильных кислот) выпадает осадок гидроксида цинка:
Na2[Zn(OH)4] + 2CO2(изб) → Zn(OH)2↓ + 2NaHCO3Na2[Zn(OH)4] + 2HCl(нед) → Zn(OH)2↓ + 2NaCl + 2H2O |
6. Соли цинка (цинкаты и сульфид)
| Соединение / Свойство | Уравнения реакций и особенности |
|---|---|
| Цинкаты и комплексы |
При прокаливании гидроксокомплексов образуются средние соли (цинкаты), а при растворении цинкатов в воде — снова комплексы. Избыток кислоты полностью разрушает их:
Na2[Zn(OH)4] t°→ Na2ZnO2 + 2H2O↑Na2ZnO2 + 2H2O → Na2[Zn(OH)4] K2ZnO2 + 4HCl(изб) → 2KCl + ZnCl2 + 2H2O |
| Сульфид цинка (ZnS) |
Единственный белый сульфид тяжёлых металлов. Важно: он растворяется в сильных кислотах-неокислителях (HCl, H₂SO₄ разбавленная), в отличие от CuS, Ag₂S, HgS:
ZnS + 2HCl → ZnCl2 + H2S↑ ZnS + 8HNO3(конц.) → ZnSO4 + 8NO2↑ + 4H2O ZnS + 4NaOH + Br2 → Na2[Zn(OH)4] + S↓ + 2NaBr |
7. Соединения ртути
| Соединение | Особенности и реакции |
|---|---|
| Оксид ртути (II) (HgO) |
Красный или жёлтый порошок (в зависимости от размера частиц). При нагревании легко разлагается (именно так Лавуазье и Пристли открыли кислород):
2HgO t>400°C→ 2Hg + O2↑ |
| Гидроксид ртути (не существует) |
Гидроксид Hg(II) крайне неустойчив. При действии щелочей на соли ртути(II) сразу выпадает желтый осадок её оксида:
Hg(NO3)2 + 2NaOH → HgO↓ + 2NaNO3 + H2O |
| Соли ртути (I) |
Ртуть проявляет степени окисления +1 и +2. В степени окисления +1 образуется уникальный двухъядерный ион Hg₂²⁺, где между атомами ртути есть ковалентная связь. Пример: каломель Hg₂Cl₂.
|
8. Качественные реакции
9. Видео эксперименты
Рекомендуем посмотреть опыты с цинком и ртутью на канале Thoisoi: