Основания и амфотерные гидроксиды: Классификация, Свойства, Получение
В этом разделе
Подробный разбор классификации, физических и химических свойств, а также способов получения оснований и амфотерных гидроксидов.
1. Классификация оснований и гидроксидов
Основания (гидроксиды) — это сложные вещества, состоящие из катиона металла (или иона аммония NH₄⁺) и одной или нескольких гидроксильных групп OH⁻.
По растворимости в воде:
- Растворимые (Щёлочи): Образованы щелочными (Li, Na, K, Rb, Cs) и щелочноземельными (Ca, Sr, Ba) металлами. Являются сильными электролитами.
- Нерастворимые: Гидроксиды большинства других металлов (Cu, Fe, Zn, Al и др.). Являются слабыми электролитами.
По химическим свойствам:
- Основные гидроксиды: Проявляют только основные свойства (реагируют с кислотами). Характерны для металлов в с.о. +1, +2.
- Амфотерные гидроксиды: Проявляют двойственные свойства (реагируют и с кислотами, и со щелочами). Характерны для металлов в с.о. +3, +4 (а также Zn+2, Be+2, Pb+2, Sn+2).
По кислотности (числу групп OH):
- Однокислотные (NaOH, KOH)
- Двухкислотные (Ca(OH)₂, Cu(OH)₂)
- Трехкислотные (Fe(OH)₃, Al(OH)₃)
2. Физические свойства
Большинство оснований — твердые вещества различного цвета.
| Формула | Название / Физические свойства / Фото | ||
|---|---|---|---|
| Щёлочи | |||
| NaOH | Название: Гидроксид натрия (Едкий натр, каустик) Физические свойства: Белое твердое вещество, очень гигроскопично, мылкое на ощупь, разъедает кожу. Фото:  | ||
| KOH | Название: Гидроксид калия (Едкое кали) Физические свойства: Белые кристаллы, очень гигроскопичны. Фото:  | ||
| Ca(OH)₂ | Название: Гидроксид кальция (Гашеная известь) Физические свойства: Белый рыхлый порошок, малорастворим (известковая вода — насыщенный раствор). Фото:  | ||
| Ba(OH)₂ | Название: Гидроксид бария Физические свойства: Белые кристаллы, хорошо растворимы. Фото:  | ||
| Нерастворимые основания | |||
| Cu(OH)₂ | Название: Гидроксид меди(II) Физические свойства: Студенистый осадок голубого цвета. Фото:  | ||
| Co(OH)₂ | Название: Гидроксид кобальта(II) Физические свойства: Сиреневый осадок. Фото:  | ||
| Fe(OH)₂ | Название: Гидроксид железа(II) Физические свойства: Белый (или зеленоватый) осадок, быстро темнеющий (буреющий) на воздухе. Фото:  | ||
| Mg(OH)₂ | Название: Гидроксид магния Физические свойства: Белое аморфное вещество. Фото:  | ||
| Ni(OH)₂ | Название: Гидроксид никеля(II) Физические свойства: Светло-зеленый осадок. Фото: 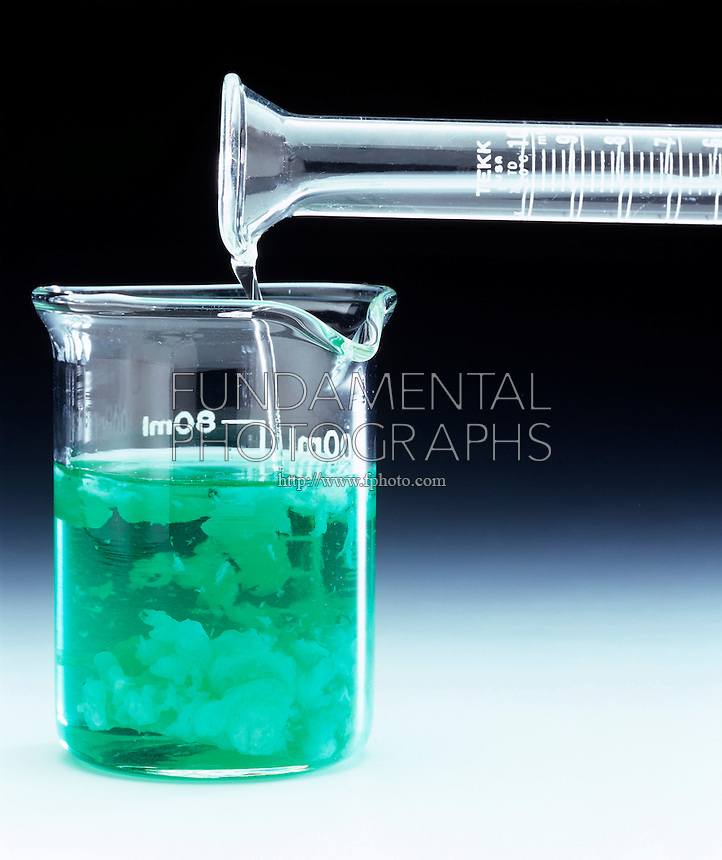 | ||
| Амфотерные гидроксиды | |||
| Al(OH)₃ | Название: Гидроксид алюминия Физические свойства: Белый желеобразный осадок. Фото:  | ||
| Zn(OH)₂ | Название: Гидроксид цинка Физические свойства: Белый осадок. Фото:  | ||
| Fe(OH)₃ | Название: Гидроксид железа(III) Физические свойства: Красно-бурый (ржавый) осадок. Фото:  | ||
| Cr(OH)₃ | Название: Гидроксид хрома(III) Физические свойства: Серо-зеленый осадок. Фото:  | ||
3. Получение оснований и амфотерных гидроксидов
| Способ получения | Примеры реакций и условия |
|---|---|
| 1. Получение щелочей | |
| Взаимодействие металлов с водой |
Щелочные и щелочноземельные металлы реагируют с водой:
2Na + 2H2O → 2NaOH + H2↑Ca + 2H2O → Ca(OH)2 + H2↑
До (Кальций)

После (Выделение H₂)
 |
| Взаимодействие оксидов с водой |
Оксиды щелочных и щелочноземельных металлов:
Li2O + H2O → 2LiOHBaO + H2O → Ba(OH)2 |
| Электролиз растворов солей |
Чаще всего используются растворы хлоридов:
2NaCl + 2H2O эл.→ 2NaOH
+ H2↑ + Cl2↑
|
| Обменные реакции |
Взаимодействие солей с другими щелочами (если образуется осадок):
K2CO3 + Ca(OH)2 →
CaCO3↓ + 2KOH (каустификация поташа)
|
| 2. Получение нерастворимых и амфотерных гидроксидов | |
| Взаимодействие солей со щелочами |
К раствору соли металла приливают щелочь (образуется осадок гидроксида):
CuCl2 + 2NaOH → Cu(OH)2↓ + 2NaCl
До (CuCl₂ + NaOH)

После (Cu(OH)₂↓)
 FeSO4 + 2KOH → Fe(OH)2↓ + K2SO4
До (FeSO₄)

После (Fe(OH)₂↓)
 AlCl3 + 3NaOH(недостаток) → Al(OH)3↓ + 3NaCl ZnSO4 + 2KOH(недостаток) → Zn(OH)2↓ + K2SO4
Важно: При получении амфотерных гидроксидов избегают избытка
щелочи, так как осадок растворится с образованием комплексов.
|
4. Химические свойства оснований и амфотерных гидроксидов
4.1. Химические свойства щелочей
\n \n
| Свойство | Реакция |
|---|---|
| 1. Диссоциация в растворе |
Щелочи (сильные электролиты) полностью распадаются на ион металла и гидроксид-ион:
NaOH → Na⁺ + OH⁻Изменяют цвет индикаторов: лакмус — синий, фенолфталеин — малиновый, метилоранж — желтый.
NaOH + ф/ф (Малиновый)
 |
| 2. Взаимодействие с кислотными оксидами |
При недостатке кислотного оксида образуется средняя соль и вода:
CO₂ + 2NaOH → Na₂CO₃ + H₂OP₂O₅ + 6KOH → 2K₃PO₄ + 3H₂O При избытке кислотного оксида образуется кислая соль (если позволяет валентность):
SO₂ + Ca(OH)₂ (изб.) → CaSO₃↓ + H₂O2SO₂ (изб.) + Ca(OH)₂ → Ca(HSO₃)₂ SiO₂ реагирует со щелочами только при сплавлении:
SiO₂ + 2NaOH t°→ Na₂SiO₃ + H₂O
|
| 3. Взаимодействие с кислотами |
Типичная реакция нейтрализации. Образуется соль и вода:
NaOH + HCl → NaCl + H₂O2KOH + H₂S → K₂S + 2H₂O При избытке многоосновной кислоты получаются кислые соли:
KOH + H₂SO₄ (изб.) → KHSO₄ + H₂O3NaOH + H₃PO₄ → Na₃PO₄ + 3H₂O |
| 4. Взаимодействие с амфотерными оксидами |
В расплаве амфотерный оксид вытесняет воду, образуя безводные средние соли (алюминаты, цинкаты): Al₂O₃ + 2KOH t°→ 2KAlO₂ + H₂O В растворе образуются комплексные соли (с квадратными скобками): ZnO + 2NaOH + H₂O → Na₂[Zn(OH)₄] |
| 5. Взаимодействие с амфотерными гидроксидами |
В расплаве отщепляется вода и образуется средняя соль: Al(OH)₃ + KOH t°→ KAlO₂ + 2H₂O В растворе гидроксид "растворяется" в избытке щелочи (образование комплекса): Zn(OH)₂ + 2NaOH → Na₂[Zn(OH)₄] |
| 6. Взаимодействие с солями |
Реакция обмена идет только если образуется осадок или газ:
CuCl₂ + Ca(OH)₂ → CaCl₂ + Cu(OH)₂↓NH₄Cl + KOH → NH₃↑ + H₂O + KCl
До (Соли)

После (Выделение NH₃)
 Щелочи переводят кислые соли в средние:
KHCO₃ + KOH → K₂CO₃ + H₂OПри взаимодействии с солями амфотерных металлов результат зависит от пропорций:
AlCl₃ + 3NaOH (недост.) → Al(OH)₃↓ + 3NaClAlCl₃ + 4NaOH (изб.) → Na[Al(OH)₄] + 3NaCl |
| 7. Взаимодействие с металлами |
Щелочи растворяют амфотерные металлы (Al, Zn, Be), выделяя водород и образуя комплекс:
2Al + 2NaOH + 6H₂O → 2Na[Al(OH)₄] + 3H₂↑
До (Al и щелочь)

После (Бурное растворение)
 Zn + 2KOH + 2H₂O → K₂[Zn(OH)₄] + H₂↑ Be + 2LiOH + 2H₂O → Li₂[Be(OH)₄] + H₂↑ |
| 8. Взаимодействие с неметаллами |
Диспропорционирование галогенов (кроме фтора), серы и фосфора:
3S + 6NaOH t°→ Na₂SO₃ + 2Na₂S + 3H₂O4P + 3KOH + 3H₂O t°→ 3KH₂PO₂ + PH₃↑ Кремний окисляется щелочью без диспропорционирования:
Si + 2KOH + H₂O → K₂SiO₃ + 2H₂↑Хлор (и бром) реагируют по-разному в зависимости от температуры:
Cl₂ + 2NaOH → NaCl + NaClO + H₂O (на холоде)3Cl₂ + 6NaOH t°→ 5NaCl + NaClO₃ + 3H₂O (при нагревании) |
| 9. Взаимодействие с галогенангидридами кислот |
Полный гидролиз хлорангидридов: все связи Э–Cl рвутся, образуются две соли:
PCl₅ + 8NaOH → Na₃PO₄ + 5NaCl + 4H₂O
|
| 10. Термическое разложение |
Большинство щелочей плавятся без разложения! Разлагается только LiOH и гидроксиды щелочноземельных металлов:
2LiOH t°→ Li₂O + H₂OCa(OH)₂ t°→ CaO + H₂O (с трудом) |
4.2. Химические свойства нерастворимых оснований
\n \n
| Свойство | Реакция |
|---|---|
| 1. Взаимодействие с кислотными оксидами |
Реагируют только с оксидами самых сильных кислот (SO₃, N₂O₅). Слабые не реагируют:
SO₃ + Cu(OH)₂ → CuSO₄ + H₂O
|
| 2. Взаимодействие с кислотами (кроме H₂SiO₃) |
Осадок "растворяется" в кислоте с образованием соли и воды:
Fe(OH)₂ + 2HCl → FeCl₂ + 2H₂OCu(OH)₂ + H₂SO₄ → CuSO₄ + 2H₂O Mg(OH)₂ + 2HNO₃ → Mg(NO₃)₂ + 2H₂O |
| 3. Термическое разложение |
При нагревании нерастворимые основания легко теряют воду:
Cu(OH)₂ t°→ CuO + H₂OMg(OH)₂ t°→ MgO + H₂O 2Fe(OH)₃ t°→ Fe₂O₃ + 3H₂O |
| 4. Специфические свойства |
Окисление гидроксида железа (II) со сменой цвета с белого на бурый:
2Fe(OH)₂ + H₂O₂ → 2Fe(OH)₃4Fe(OH)₂ + O₂ + 2H₂O → 4Fe(OH)₃
До (Fe(OH)₂)

После (Fe(OH)₃)
 Растворение осадка в избытке аммиака (образование аммиаката):
Cu(OH)₂ + 4NH₃ · H₂O → [Cu(NH₃)₄](OH)₂ + 4H₂O
До (Осадок Cu(OH)₂)

После (Раствор)
 |
4.3. Химические свойства амфотерных гидроксидов
\n \n
| Свойство | Пример реакции |
|---|---|
| Взаимодействие с кислотными оксидами |
Проявляют основные свойства, реагируют с оксидами сильных кислот:
2Al(OH)₃ + 3SO₃ → Al₂(SO₄)₃ + 3H₂O
|
| Взаимодействие с кислотами |
Растворяются в кислотах по основному типу (соль + вода):
Zn(OH)₂ + 2HCl → ZnCl₂ + 2H₂O2Al(OH)₃ + 3H₂SO₄ → Al₂(SO₄)₃ + 6H₂O |
| Взаимодействие с основными оксидами |
Проявляют кислотные свойства. Реакция идет только при сплавлении:
2Al(OH)₃ + Na₂O t°→ 2NaAlO₂ + 3H₂O
|
| Взаимодействие со щелочами |
При сплавлении образуют безводные средние соли и воду:
Fe(OH)₃ + KOH t°→ KFeO₂ + 2H₂OCr(OH)₃ + NaOH t°→ NaCrO₂ + 2H₂O В растворе образуют комплексные соли (Внимание: Fe(OH)₃ в растворе щелочи не растворяется!):
Be(OH)₂ + 2NaOH → Na₂[Be(OH)₄]Zn(OH)₂ + 2KOH → K₂[Zn(OH)₄] Al(OH)₃ + NaOH → Na[Al(OH)₄]
До (Осадок Al(OH)₃)

После (Раствор)
 |
| Взаимодействие с карбонатами |
Амфотерные гидроксиды вытесняют летучие кислотные оксиды из солей при сплавлении:
Na₂CO₃ + Zn(OH)₂ t°→ Na₂ZnO₂ + CO₂↑ + H₂O
|
| Термическое разложение |
Как и нерастворимые основания, разлагаются на оксид и воду при прокаливании:
2Fe(OH)₃ t°→ Fe₂O₃ + 3H₂O2Al(OH)₃ t°→ Al₂O₃ + 3H₂O |
| Окислительно-восстановительные реакции |
Соединения Cr(III) и Fe(III) могут быть окислены в щелочной среде до Cr(VI) и Fe(VI):
2Cr(OH)₃ + 3H₂O₂ + 4NaOH → 2Na₂CrO₄ (желтый) + 8H₂O
До (Осадок Cr(+3))

После (Раствор Cr(+6))
 2Fe(OH)₃ + 3Br₂ + 10KOH → 2K₂FeO₄ (красно-фиолетовый) + 6KBr + 8H₂O
До (Осадок Fe(+3))

После (Феррат Fe(+6))
 |
4.4. Химические свойства гидроксида аммония
\n \n
| Свойство | Реакция |
|---|---|
| 1. Диссоциация в растворе |
Раствор аммиака проявляет свойства слабого основания, диссоциирует обратимо:
NH₃ · H₂O ⇄ NH₄⁺ + OH⁻Изменяет цвет индикаторов, среда раствора — слабощелочная. |
| 2. Осаждение из солей |
Как основание, осаждает нерастворимые гидроксиды металлов из растворов их солей:
AlCl₃ + 3NH₃ · H₂O → Al(OH)₃↓ + 3NH₄ClFeSO₄ + 2NH₃ · H₂O → Fe(OH)₂↓ + (NH₄)₂SO₄ Cr(NO₃)₃ + 3NH₃ · H₂O → Cr(OH)₃↓ + 3NH₄NO₃ |
| 3. Образование аммиакатов |
Гидроксиды некоторых металлов (Cu, Ag, Zn) способны переходить в раствор в избытке аммиака:
Cu(OH)₂ + 4NH₃ · H₂O → [Cu(NH₃)₄](OH)₂ + 4H₂O (ярко-синий)Ag₂O + 4NH₃ · H₂O → 2[Ag(NH₃)₂]OH + 3H₂O Zn(OH)₂ + 4NH₃ · H₂O → [Zn(NH₃)₄](OH)₂ + 4H₂O |